P, p - сопряженные системы. Простейший пример бутадиен – 1,3. Все атомы в бутадиене находятся в SP2 – гибридизированном состоянии и лежат в одной плоскости. Рz – орбитали параллельны друг другу. Это создает условия их взаимного перекрывания. Перекрывание Рz орбитали происходит между С-1 и С-2 и С-3 и С-4, а также между С-2 и С-3, то есть возникает делокализованная ковалентная связь. Это находит отражение в изменении длин связей в молекуле бутадиена-1.3. Длина связи между С-1 и С-2 увеличена, а между С-2 и С-3 укорочена, по сравнению с одинарной связью.
Различают p,p и r,p сопряженные системы. Рассмотрим каждую из них.
Чаще всего мы с вами будем иметь дело с сопряженными системами. Если же двойные связи чередуются с одинарными связями, такие системы называются сопряженными.
Например, в олеиновой кислоте ковалентная связь локализованная.
Двойная связь характерна ненасыщенным соединениям, в которых, кроме центровой s - связи, есть еще связь, которая называется пи - связью.
Двойные связи бывают локализованными, то есть электронная плотность охватывает только 2 ядра связываемых атомов.
СН3 – (СН2)7 – СН = СН – (СН2)7 – СООН
Например:
СН2 = СН – СН = СН2
l- C -С, 154 нм l- С=С = 0,134 нм, l- С=С =0.120 нм
Примером р, π сопряженной системы может служить пептидная связь.
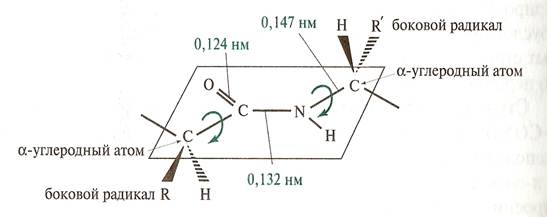
Двойная связь С=0 удлинняется до 0,124 нм против обычной длины 0,121, а связь С – N становится короче и становится равной 0,132 нм по сравнению с 0,147 нм в обычном случае. То есть процесс делокализации электронов приводит к выравниванию длин связей и снижению внутренней энергии молекулы. Однако ρ,p – сопряжение возникает в ациклических соединениях, когда чередуется = связи с С- С связями и с гетероатомом:
 Например: О О
Например: О О
 СН2 = СН– С СН2 = СН – С
СН2 = СН– С СН2 = СН – С
Н ОН
пропеналь акриловая кислота
Рядом с двойной связью может находиться атом Х, имеющий свободную р- орбиталь. Чаще всего это гетероатомы О,N, S и их р-орбитали, взаимодействуют р-орбитали с p - связями, образуя р, p - сопряжение.
Например:
СН2 = СН – О – СН = СН2
Сопряжение может осуществляться не только в нейтральных молекулах, но и в радикалах и ионах:
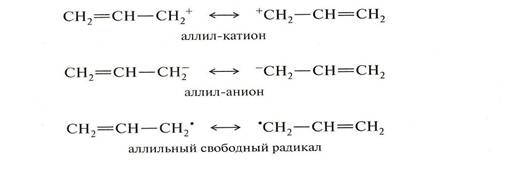
Итак, исходя из выше изложенного, в открытых системах сопряжение возникает при следующих условиях:
А) Все атомы, участвующие в сопряженной системе, находятся в SP2 – гибридизованном состоянии.
Б) Р z – орбитали всех атомов перпендикулярны плоскости s - связи, то есть параллельны друг другу.
При образовании сопряженной многоцентровой системы происходит выравнивание длин связей. Здесь нет «чистых» одинарных и двойных связей.
Делокализация p- электронов в сопряженной системе сопровождается выделением энергии. Система переходит на более низкий энергетический уровень, становится более устойчивой, более стабильной. Так, образование сопряженной системы в случае бутадиена – 1,3 приводит к выбросу энергии в количестве 15 кДж/моль. Именно за счет сопряжения повышается устойчивость радикалов ионов аллильного типа и их распространенность в природе.
Чем длиннее цепь сопряжения, тем больше выброс энергии ее образования.
Это явление довольно широко распространено в биологически важных соединениях.
Например:
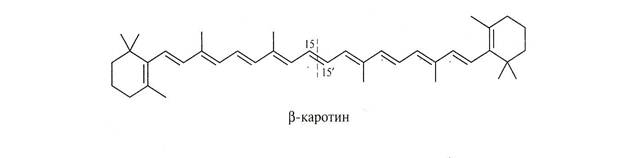
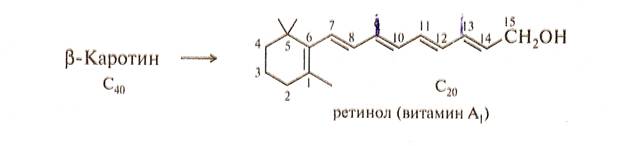
При окислении бета каротинов образуются витамин А и ретиналь.
С вопросами термодинамической устойчивости молекул, ионов, радикалов мы будем постоянно встречаться в курсе биоорганической химии, к которым относятся ряд ионов и молекул широко распространенных в природе..
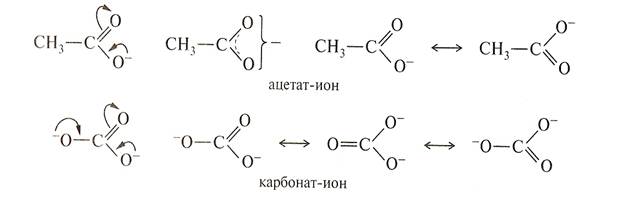
Сопряженные системы с замкнутой цепью.
Ароматичность. В циклических молекулах при определенных условиях может возникать сопряженная система. Примером p, p - сопряженной системы является бензол, где p - электронное облако охватывает часть атомов углерода, такая система называется – ароматической.
Выигрыш энергии сопряжения в бензоле составляет 150,6 кДж/моль. Поэтому бензол устойчив термически до температуры 900оС.
Наличие замкнутого электронного кольца доказано с помощью ЯМР. Если молекулу бензола поместить во внешнее магнитное поле, возникает индуктивный кольцевой ток.
Таким образом, критерием ароматичности, сформулированным Хюккелем является:
А) молекула имеет циклическое строение;
Б) все атомы находятся в SP2 – гибридизованном состоянии;
В) существует делокализиванная p - электронная система, содержащая 4n + 2 электронов, где n – число циклов.
Например:
Особое место в биоорганической химии занимает вопрос ароматичности гетероциклических соединений.
В циклических молекулах, содержащих гетероатомы (азот, сера, кислород) единое p - электронное облако, образуется с участием р – орбиталей атомов углерода и гетероатома.
 2014-02-13
2014-02-13 2117
2117
