Валентность
Важной количественной характеристикой, показывающей число взаимодействующих между собой атомов в образовавшейся молекуле, является валентность – свойство атомов одного элемента присоединять определенное число атомов других элементов.
Количественно валентность определяется числом атомов водорода, которое данный элемент может присоединять или замещать. Так, например, в плавиковой кислоте (HF) фтор одновалентен, в аммиаке (NH3) азот трехвалентен, в кремневодороде (SiH4 – силан) кремний четырехвалентен и т.д.
Позже, с развитием представлений о строении атомов, валентность элементов стали связывать с числом неспаренных электронов (валентных), благодаря которым осуществляется связь между атомами. Таким образом, валентностьопределяется числом неспаренных электронов в атоме, принимающих участие в образовании химической связи (в основном или возбужденном состоянии). В общем случае валентность равна числу электронных пар, связывающих данный атом с атомами других элементов.
Трудности определения валентности в сложных молекулах привели исследователей к необходимости ввести понятие о степени окисления – величине формальной, но легко рассчитываемой. Степенью окисления принято называть условный заряд атома в молекуле, который возникает за счет смещения электронной плотности от менее к более электроотрицательному атому. Степень окисления может иметь отрицательное, положительное и нулевое значения, которые обычно выражают арабскими цифрами со знаком «+» или «-» и ставят над символом элемента. Например, 
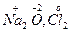
Отрицательную степень окисления имеют атомы, которые приняли электроны от других атомов, т.е. в их сторону смещено связующее электронное облако. Отрицательную степень окисления (-1) имеет атом фтора во всех своих соединениях.
Положительную степень окисления имеют атомы, отдающие свои электроны другим атомам, т.е. связующее электронное облако оттянуто от них. К таковым относятся металлы в соединениях. Степень окисления щелочных металлов равна (+1), а щелочноземельных – (+2).
Нулевую степень окисления имеют атомы в молекулах простых веществ, например водорода, хлора, азота, т.к. в этом случае связующее электронное облако в равной мере принадлежит обоим атомам. Если вещество находится в атомарном состоянии, то степень окисления его атомов также равна нулю.
В большинстве соединений атомы водорода имеют степень окисления (+1), только в гидридах металлов, например, NaH, CaH2, она равна (-1). Кислород в большинстве соединений имеет степень окисления (-2), но в соединении с фтором (F2O) она равна (+2), в пероксидах – (-1). Пользуясь этими сведениями можно вычислить степень окисления атомов в сложных соединениях, учитывая, что алгебраическая сумма степеней окисления атомов в соединении всегда равна нулю, а в сложном ионе – заряду иона.
 2014-02-18
2014-02-18 1210
1210