Рис. 93. Схема цепи, поясняющая принцип работы стеклянного электрода
Стеклянный электрод имеет ряд существенных преимуществ по сравнению с водородным электродом, с помощью которого тоже можно измерять концентрацию ионов Н+ в растворе.
Он совершенно не чувствителен к различным примесям в растворе, «не отравляется ими», им можно пользоваться, если в анализируемых жидкостях содержатся сильные окислители и восстановители, а также в самом широком диапазоне значений рН – от 0 до 12. Недостатком стеклянного электрода является его большая хрупкость.
Химические источники электрического тока или гальванические элементы преобразуют энергию, выделяющуюся при протекании окислительно-восстановительных реакций, в электрическую энергию. Гальванические элементы служат источниками постоянного тока. Они подразделяются на химические и концентрационные.
Простейший химический гальванический элемент можно составить из двух металлических электродов, имеющих различные электродные потенциалы, и соединенных в замкнутую цепь.
На электроде, который имеет меньшее значение электродного потенциала, будет происходить процесс окисления. Такой электрод называется иначе анодом.
На электроде, который имеет большее значение электродного потенциала, будет происходить процесс восстановления. Такой электрод называется иначе катодом.
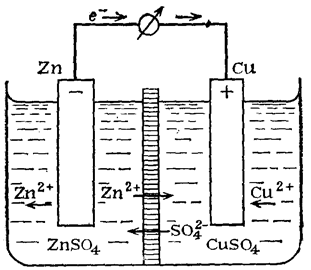
Рассмотрим более подробно принцип работы гальванических элементов на примере элемента, составленного из цинкового и медного электродов. Такой элемент называется иначе элементом Якоби-Даниэля (рис. 94).
 2014-02-09
2014-02-09 797
797








