Структура микроэмульсий и мицеллярных растворов. Термодинамика мицеллообразования. Фазовые диаграммы растворов ПАВ. Мицеллярный катализ.
Лимитирующие стадии. Обмен через дисперсионную среду. Одночастичный обмен при столкновении мицелл. Механизм обмена типа "слияние-разделение". Обобщенная модель столкновительного комплекса. Кинетика тушения люминесценции в мицеллах.
В данной главе мы рассмотрим основные закономерности протекания химических и фотохимических реакций в мицеллярных растворах и микроэмульсиях. Основной структурообразующей единицей в этих системах являются молекулы амфифильных веществ (АФ) или, как их чаще называют – поверхностно-активных веществ (ПАВ). Такое название отражает их свойство концентрироваться на поверхности раздела фаз несмешивающихся жидкостей.
Специфические физико-химические свойства ПАВ обусловлены их асиметричным строением, молекулы ПАВ состоят из гидрофильной части, т.е. «любящей воду», и гидрофобной, или олеофильной части, т.е. «любящей масло». Можно привести ряд примеров. Хорошо известен класс детергентов, которые представляют собой соли жирных кислот, имеющих в своем составе гибкую парафиновую цепочку CnH2n+1 – алкильный (или еще говорят) хвост, присоединенный к полярной группе, в качестве которой могут выступать ¾ OSO3Na, ¾ NH3Cl, ¾ COOK и т.п. В полярном растворителе эти группы могут полностью или частично диссоциировать.
К наиболее широко известным ПАВ относится, например, додецилсульфат натрия C12H25 ¾ OSO3Na (SDS). Обычное мыло представляет собой смесь натриевых солей стеариновой и пальмитиновой кислот. SDS и другие аналогичные ПАВ обладают свойством образовывать в гидрофильной среде (в частности, в воде) агрегаты, называемые мицеллами (рис. 1), в которых гидрофильные части молекул ПАВ находятся на поверхности мицеллы и непосредственно контактируют с полярным растворителем, а хвосты образуют гидрофобное ядро мицеллы.
Другим широко используемым ПАВ является молекула так называемого аэрозоля ОТ (АОТ), имеющая следующую структурную формулу:
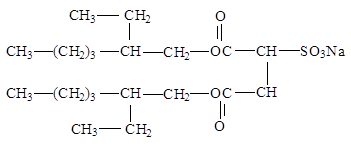
Молекула АОТ имеет два алкильных хвоста и часто используется для стабилизации микроэмульсий типа «вода в масле». Другим интересным свойством молекулы АОТ является способность образовывать в гидрофобной среде так называемые обратные мицеллы (рис. 1). В живой природе важную роль играют липиды, например, холестерин, и фосфолипиды, например, различные лецитины, общая структурная формула которых имеет вид
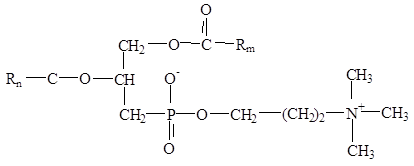
где Rn и Rm – парафиновые цепочки. Лецитины в полярных средах образуют бислойные структуры (ламеллы), строение которых аналогично структуре клеточных мембран (рис. 1). Еще одной характерной структурой, которую образуют фосфолипиды в полярной среде, являются везикулы – пузырек, в который сворачивается бислойная мембрана (рис. 1).
Амфифильный характер молекул ПАВ позволяет независимо оценить вклады гидрофильной и гидрофобной частей в изменение свободной энергии раствора, вызванного добавлением одной молекулы ПАВ в растворитель. Гидрофильная группа молекул ПАВ притягивает к себе молекулы воды, что приводит к понижению свободной энергии системы. С другой стороны, жирный хвост молекулы ПАВ в полярном растворителе вызывает понижение энтропии жидкости вблизи молекулы ПАВ, т.е. увеличивает свободную энергию раствора. В неполярных средах энергия сольватации гидрофильной части молекулы мала, зато гидрофобная часть дает понижение свободной энергии системы, как бы следуя эмпирическому правилу химии: «подобное растворяется в подобном». Конечно, такое разделение имеет смысл для достаточно больших молекул, имеющих хорошо выраженные полярный и неполярный фрагменты. Соотношение этих вкладов в свободную энергию характеризует так называемый гидрофильно-гидрофобный баланс молекулы ПАВ. Амфифильный характер имеют молекулы спиртов, которые сами по себе не являются поверхностно-активными веществами и не могут образовывать мицеллы и другие подобные структуры. Однако они могут существенно изменить свойства ПАВ, тем самым влияя на структуру и динамику мицеллярных растворов и микроэмульсий.
Таким образом, наиболее благоприятным местом расположения молекул ПАВ в гетерофазных системах является граница поверхности раздела. В этом случае свободная энергия системы уменьшается как за счет гидрофобного взаимодействия жирных хвостов так и за счет выигрыша энергии сольватации полярной части молекулы.
 2014-02-09
2014-02-09 1473
1473