Москва 2006
РОССИЙСКИЙ УНИВЕРСИТЕТ ДРУЖБЫ НАРОДОВ
Значения статистик Дарбина-Уотсона при 5%-ном уровне значимости
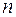 | 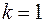 | 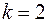 | 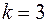 | 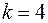 | 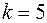 | |||||
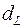 | 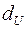 | 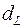 | 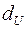 | 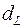 | 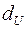 | 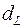 | 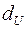 | 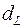 | 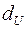 | |
| 0,61 | 1,40 | |||||||||
| 0,70 | 1,36 | 0,47 | 1,90 | |||||||
| 0,76 | 1,33 | 0,56 | 1,78 | 0,37 | 2,29 | |||||
| 0,82 | 1,32 | 0,63 | 1,70 | 0,46 | 2,13 | |||||
| 0,88 | 1,32 | 0,70 | 1,64 | 0,53 | 2,02 | |||||
| 0,93 | 1,32 | 0,66 | 1,60 | 0,60 | 1,93 | |||||
| 0,97 | 1,33 | 0,81 | 1,58 | 0,66 | 1,86 | |||||
| 1,01 | 1,34 | 0,86 | 1,56 | 0,72 | 1,82 | |||||
| 1,05 | 1,35 | 0,91 | 1,55 | 0,77 | 1,78 | |||||
| 1,08 | 1,36 | 0,95 | 1,54 | 0,82 | 1,75 | 0,69 | 1,97 | 0,56 | 2,21 | |
| 1,10 | 1,37 | 0,98 | 1,54 | 0,86 | 1,73 | 0,74 | 1,93 | 0,62 | 2,15 | |
| 1,13 | 1,38 | 1,02 | 1,54 | 0,90 | 1,71 | 0,78 | 1,90 | 0,67 | 2,10 | |
| 1,16 | 1,39 | 1,05 | 1,53 | 0,93 | 1,69 | 0,82 | 1,87 | 0,71 | 2,06 | |
| 1,18 | 1,40 | 1,08 | 1,53 | 0,97 | 1,68 | 0,85 | 1,85 | 0,75 | 2,02 | |
| 1,20 | 1,41 | 1,10 | 1,54 | 1,00 | 1,68 | 0,90 | 1,83 | 0,79 | 1,99 | |
| 1,22 | 1,42 | 1,13 | 1,54 | 1,03 | 1,67 | 0,93 | 1,81 | 0,83 | 1,96 | |
| 1,24 | 1,43 | 1,15 | 1,54 | 1,05 | 1,66 | 0,96 | 1,80 | 0,86 | 1,94 | |
| 1,26 | 1,44 | 1,17 | 1,54 | 1,08 | 1,66 | 0,99 | 1,79 | 0,90 | 1,92 | |
| 1,27 | 1,45 | 1,19 | 1,55 | 1,10 | 1,66 | 1,01 | 1,78 | 0,93 | 1,99 | |
| 1,29 | 1,45 | 1,21 | 1,55 | 1,12 | 1,66 | 1,04 | 1,77 | 0,95 | 1,89 | |
| 1,30 | 1,46 | 1,22 | 1,55 | 1,14 | 1,65 | 1,06 | 1,76 | 0,98 | 1,88 | |
| 1,32 | 1,47 | 1,24 | 1,56 | 1,16 | 1,65 | 1,08 | 1,76 | 1,01 | 1,86 | |
| 1,33 | 1,48 | 1,26 | 1,56 | 1,18 | 1,65 | 1,10 | 1,75 | 1,03 | 1,85 | |
| 1,34 | 1,48 | 1,27 | 1,56 | 1,20 | 1,65 | 1,12 | 1,74 | 1,05 | 1,84 | |
| 1,35 | 1,49 | 1,28 | 1,57 | 1,21 | 1,65 | 1,14 | 1,74 | 1,07 | 1,83 |
В.А. Туриков
КОНСПЕКТ ЛЕКЦИЙ ПО МОЛЕКУЛЯРНОЙ ФИЗИКЕ ДЛЯ СПЕЦИАЛЬНОСТЕЙ «ФИЗИКА» И «РАДИОФИЗИКА И ЭЛЕКТРОНИКА»
Термодинамические параметры (параметры состояния): 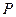 - давление,
- давление, 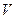 - объем,
- объем, 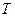 - температура.
- температура.
Температура – мера нагретости тела. Для измерения температуры используют различные свойства тел при нагревании. Например, в ртутном термометре используется свойство ртути расширяться при нагревании. Другой метод измерения температуры, термопара, основан на явлении возникновения термоэлектродвижущей силы в цепи из двух различных спаянных проводников, концы которых находятся при различной температуре. Существует множество других методов измерения температуры.
Шкала температур определяется заданием двух основных температурных точек (реперные точки). В шкале Цельсия такими точками являются температура плавления льда (00 С) и температура кипения воды (1000 С) при нормальном атмосферном давлении. Абсолютная шкала температур (шкала Кельвина) связана со шкалой Цельсия соотношением 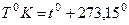 . Физический смысл абсолютной шкалы температур будет рассмотрен далее.
. Физический смысл абсолютной шкалы температур будет рассмотрен далее.
За единицу давления в системе СИ принимается 1 паскаль (Па), равный давлению, при котором на 1 м2 поверхности нормально к ней действует сила в 1 ньютон. Используется также внесистемная единица измерения – 1 атмосфера (атм), равная давлению столба ртути высотой 760 мм (1 атм = 101325 Па). Часто давление измеряется просто в мм ртутного столба. При низких давлениях используют единицу 1 тор, равную 1 мм ртутного столба.
Идеальным газом будем называть газ, строго подчиняющийся эмпирическим законам Бойля-Мариотта, Шарля и Гей-Люссака. С молекулярно-кинетической точки зрения в таком газе можно пренебречь энергией взаимодействия молекул по сравнению с кинетической энергией их теплового движения. Эмпирические законы идеальных газов описывают изопроцессы, в которых один из трех термодинамических параметров остается постоянным. Во всех этих законах масса газа считается неизменной.
1. Изотермический процесс (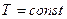 ).
).
2. Изохорический процесс (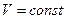 ).
).
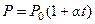 (закон Шарля).
(закон Шарля).
Здесь 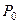 - давление газа при
- давление газа при 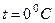 ,
, 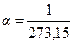 град–1.
град–1.
3. Изобарический процесс (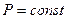 ).
).
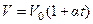 (закон Гей-Люссака),
(закон Гей-Люссака),
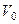 - объем газа при
- объем газа при 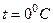 .
.
Два последних закона можно записать в другом виде. Например, из закона Шарля следует
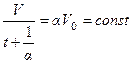 .
.
Отсюда становится понятным возникновение слагаемого 273,15 в определении абсолютной температуры. Таким образом законы Шарля и Гей-Люссака принимают вид
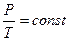 ,
, 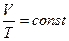 .
.
Можно объединить эти три закона и записать их в виде уравнения Клапейрона
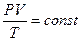 при постоянной массе газа.
при постоянной массе газа.
 2014-02-09
2014-02-09 3218
3218
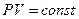 (
(






