СВОЙСТВА МЕТАЛЛОВ
Все простые вещества можно разделить на металлы и неметаллы изза существенного различия их свойств (табл. 11.1).
Таблица 11.1
Некоторые характерные свойства металлов и неметаллов
| Характерные свойства | |
| металлов | неметаллов |
| Металлическая связь в кристаллах | Ковалентная связь в большинстве простых веществ |
| Металлический блеск | Различается окраска |
| Хорошие теплопроводность и электрическая проводимость | Плохие теплопроводность и электрическая проводимость |
| Ковкость и пластичность | Хрупкость твердых тел (как правило) |
| Восстановители | Многие из них окислители |
| Большинство оксидов – ионные соединения, имеют основной характер и при растворении в воде образуют основные растворы | Большинство оксидов – ковалентные соединения, имеют кислотный характер и при растворении в воде образуют кислотные растворы |
Большинство элементов являются металлами. К ним относятся все s -элементы, кроме водорода и гелия, все d- и f – элементы и часть р – элементов (Al, Ga, In, Tl, Sn, Pb, Bi, Po). Металлическими свойствами обладают и многочисленные сплавы указанных элементов. Если условно провести границу от Li к At, то всё, что находится слева от этой линии – металлы, а справа - неметаллы (р – элементы).
Граница между металлами и неметаллами размыта, между ними находятся полуметаллы (B, Si, Ge, As, Sb, Te, At). Полуметаллы обладают свойствами как металлов, так и неметаллов. Например, серый мышьяк имеет металлический блеск и электрическую проводимость, но хрупок, а желтый мышьяк имеет чисто неметаллические свойства.
Металлы – простые вещества, обладающие рядом ценных для человека специфических свойств (так называемых металлических свойств).
Для металлов в конденсированном состоянии характерна кристаллическая решётка с металлической связью. Для описания металлической связи часто используют модель «свободного электрона» (см. раздел 3.9). Согласно этой модели, в узлах кристаллической решётки металла находятся положительные ионы металла, «погружённые» в электронный газ из нелокализованных валентных электронов атомов, участвующих в образовании кристалла. Устойчивость кристалла обеспечивается силами притяжения между положительными ионами и электронным газом. Именно металлической связью объясняются физические свойства металлов.
Для всех металлов (кроме ртути) характерно твердое агрегатное состояние. Твердость их различна и обусловливается прочностью пространственной кристаллической решетки. Наиболее твердые – простые вещества d-элементов VI группы, наименее твердые – простые вещества щелочных металлов. Твердость металлов определяет возможность использования их в качестве конструкционных и инструментальных материалов.
Для металлических тел с гладкой поверхностью характерен металлический блеск – результат отражения световых лучей. Металлический блеск обусловлен отражением световых лучей от электронного газа, который несколько выходит за границу положительно заряженных ионов. Интенсивность блеска зависит от доли поглощаемого веществом света; чем меньше света поглощает металл, тем ярче его блеск. Серебро и палладий, отличающиеся наиболее интенсивным блеском, используют для изготовления зеркал. В мелкодисперсном состоянии многие металлы (железо, платина и др.) теряют блеск, приобретают черную или серую окраску.
Наличие электронов, которые могут свободно перемещаться по объему кристалла, обеспечивает высокую электрическую проводимость и теплопроводность. Лучшими проводниками электричества являются серебро, медь, золото и алюминий, худшими – свинец и ртуть. Металлы обладают высокой теплопроводностью. Наибольшая теплопроводность - у металлов с наилучшей электрической проводимостью.
Ионы металлов в кристалле могут скользить относительно друг друга. Этим объясняется ковкость (способность к расплющиванию – можно ковать листы) и пластичность (способность вытягиваться в проволоку и ленту). Наиболее пластичны золото, серебро и медь; из 1 г золота удается получить проволоку длиной в 3км, изготовить «золотую фольгу» толщиной 0,0001 мм.
В технике металлы подразделяют на чёрные, цветные, редкоземельные и драгоценные. К черным относят железо и его сплавы, к драгоценным – золото, серебро, платину и иридий, к редкоземельным – скандий, иттрий, рений, осмий, лантаноиды совместно с лантаном. Остальные металлы, включая магний, алюминий, медь и их сплавы, относят к цветным. Кроме того, различают металлы щелочные (литий, натрий, калий, рубидий, цезий, франций) и щелочно-земельные (кальций, стронций, барий, радий).
Впромышленности металлы подразделяют на лёгкие (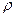 < 5 г/см3) и тяжёлые (
< 5 г/см3) и тяжёлые (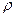 > 5 г/см3). Осмий – самый тяжёлый металл (
> 5 г/см3). Осмий – самый тяжёлый металл (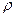 = 22,5 г/см3). По температуре плавления различают лёгкоплавкие (< 1000 оС) и тугоплавкие (> 1500 оС); самые тугоплавкий металл – вольфрам (tпл=3400 оС).
= 22,5 г/см3). По температуре плавления различают лёгкоплавкие (< 1000 оС) и тугоплавкие (> 1500 оС); самые тугоплавкий металл – вольфрам (tпл=3400 оС).
 2014-02-09
2014-02-09 1638
1638








