Факторы, влияющие на активность ферментов.
- Концентрация субстрата [S]
- Концентрация фермента [F]
- Температура
- рН
- Низкомолекулярные вещества (активаторы, ингибиторы).
Зависимость скорости ферментативной реакции субстрата выражается уравнением Михаэлиса-Ментен:
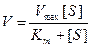
Vmax – максимальная скорость реакции
[S] – концентрация субстрата
Km – константа Михаэлиса.
Анализ уравнения Михаэлиса-Ментен.
- Концентрация субстрата мала, стремиться к нулю. При этих условиях [S] можно пренебречь:
[S]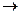 0, при этом [S] можно пренебречь:
0, при этом [S] можно пренебречь:
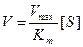
- Концентрация субстрата стремится к бесконечности, пренебрегаем Km и уравнение имеет вид:
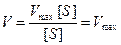
Сокращаем на [S] и скорость реакции равняется Vmax.
- Если принять, что
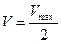 , то из уравнения Михаэлиса-Ментен, разделив его на Vmax, получили Km=[S]:
, то из уравнения Михаэлиса-Ментен, разделив его на Vmax, получили Km=[S]:
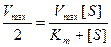 и разделив на Vmax получим
и разделив на Vmax получим 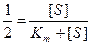 . Решая уравнение относительно Km получаем Km+[S] = 2[S],
. Решая уравнение относительно Km получаем Km+[S] = 2[S],
Km=[S]
Km – величина, численно равная концентрации субстрата при 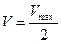 , выраженная в молях. Km = 10-1 – 10-6 – для клеток организма, величина const.
, выраженная в молях. Km = 10-1 – 10-6 – для клеток организма, величина const.
Km показывает:
- Степень сродства между ферментом и субстратом, существует обратная зависимость – чем меньше Km, тем больше сродство F к S.
- Km позволяет определить какой субстрат будет превращаться под действием данного фермента:
Например, этиленгликоль – составная часть антифриза и алкагольдегидрогеназа (АДГ) будет превращать его в щавелевую кислоту, которая является ядом для печени.
Алкагольдегидрогеназа превращает этиловый спирт в уксусный альдегид и степень сродства АДГ к С2Н5ОН выше, чем к этиленгликолю и на этом основан способ нейтрализации этиленгликоля.
- Km показывает степень сродства между белковой и небелковой частью F,
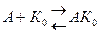
- Km позволяет определить вид ингибирования.
Способ определения Km.
- Построение график Михаэлиса-Ментен:
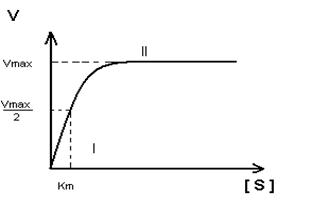
I участок – с увеличением концентрации субстрата увеличивается скорость ферментативной реакции
II участок – с увеличением концентрации субстрата скорость реакции не изменяется, т.к. все активные центры заняты.
Недостаток графика Михаэлиса-Ментен при определении Km заключается в том, что Vmax достигается с трудом, реакции в клетке протекают с оптимальной скоростью, а не Vmax.
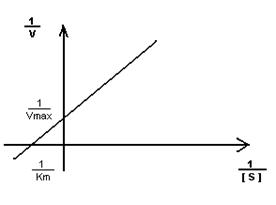
- Построение графика Лайнуэвера-Бэрка – метод обратных величин
 2014-02-12
2014-02-12 446
446








