Занятие №20.
Политропный процесс — термодинамический процесс, во время которого удельная теплоёмкость газа остаётся неизменной.
Из определения политропного процесса следует, что основные термодинамические процессы — изохорный, изобарный, изотермический и адиабатный,— если они протекают при постоянной удельной теплоемкости, являются частными случаями политропного процесса. Итак, политропный процесс проходит при постоянной теплоемкости.
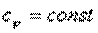
Уравнение политропного процесса имеет вид
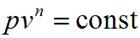
где n - показатель политропы, который изменяется для разных процессов от 0 до + бесконечности.
Рассмотренные ранее процессы являются частными случаями политропных процессов:
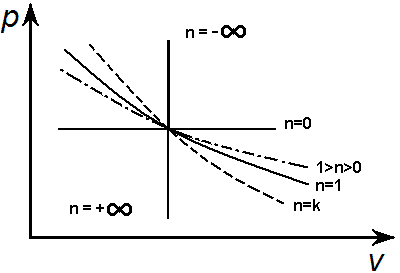
если n = к, то pvk = const — адиабатный процесс;
если n = 1, то pv1 = const — изотермический процесс;
если n = 0, то pv0 = p = const — изобарный процесс;
если n ± &, то представив pvn = const как рnv = const, имеем v =const — изохорный процесс.
Показатель изотропы n можно определить, если известны два состояния в политропном процессе:
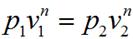
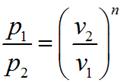
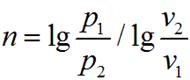 .
.
Графическое изображение политропного процесса в рv -диаграмме имеет вид кривой, которая называется политропой.
Соотношение параметров данного процесса можно получить, заменив в уравнениях адиабатного процесса показатель степени k на показатель n:
Изменение внутренней энергии в политропном процессе
для произвольной массы вещества определяется по формуле
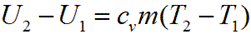
Работа изменения объема в политропном процессе для
1 кг рабочего тела равна
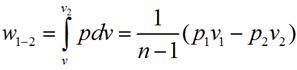
или, учитывая уравнение состояния Клапейрона,
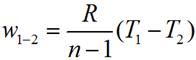
Для произвольной массы газа
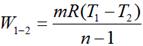
Количество теплоты в политропном процессе для m кг вещества определяется выражением, полученным в соответствии с первым законом термодинамики
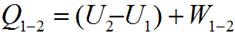
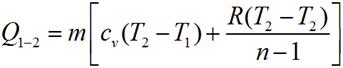
 2014-02-12
2014-02-12 8092
8092








