Динамическое равновесие наступает при достижении каждой фазой равновесной концентрации распределяемого вещества при данных условиях температуры и давления.
Сопоставление рабочих и равновесных концентраций позволяет определить скорость и направление процесса, а также характеризует движущую силу процесса, мерой которой является разность между рабочей и равновесной концентрациями.
В основе равновесия лежит правило фаз Гиббса (или закон равновесия фаз), с которым мы познакомились, рассматривая общие принципы анализа и расчета процессов и аппаратов. Как вы помните, первой из основных задач, которые приходится решать при практических расчетах процессов и аппаратов, является определение условий равновесного состояния системы. Определение направления протекания процесса в равновесных системах под действием внешней силы опирается на два основных положения термодинамики – принцип Ле-Шателье и правило фаз Гиббса. Правило фаз Гиббса, как известно, выражает зависимость между количеством компонентов системы k, фаз f и ее степеней свободы S:
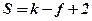 .
.
Правило фаз позволяет установить количество переменных, определяющих равновесие системы, которые могут быть выбраны произвольно (см. раздел 1.3).
 2014-02-13
2014-02-13 2394
2394
