1. Восстановитель СО. Реакции восстановления оксидов железа могут быть представлены в следующем виде:
3 Fe 2 O 3 + CO → 2 Fe 3 O 4 + CO 2; ∆H 1= - 53, 74 кДж;
Fe 3 O 4 + CO↔ 3 FeO + CO 2; ∆H 2= 36, 68 кДж;
FeO +CO↔ Fe + CO 2; ∆H 3= - 16, 26 кДж.
Эти реакции протекают последовательно при температуре выше 570°С. При более низкой температуре железо восстанавливаетсянепосредственно из магнитной окиси железа Fe 3 O 4 по реакции:
1/4 Fe 3 O 4 +CO↔ 3/4 Fe + CO 2; ∆H 4= - 2,87 кДж.
Для всех реакций 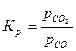 .
.
Числовые значения констант равновесия реакций восстановления железа понижаются скачком при переходе от высших оксидов к низшим.
2. Восстановитель твёрдый углерод. Реакции восстановления:
3 Fe 2 O 3 + C → 2 Fe 3 O 4 + CO; ∆H 1= 118,82 кДж;
Fe 3 O 4 + C→ 3 FeO + CO; ∆H 2= 209,26 кДж;
FeO +C→ Fe + CO; ∆H 3= 156,50 кДж.
Реакция прямого восстановления в общем виде:
МеО + С ↔ Ме + СО.
Реакция между двумя твёрдыми компонентами оксидом и твёрдым углеродом ограничивается из-за недостаточного контакта между их поверхностями и низкой скоростью диффузии углерода в твёрдом оксиде.
В условиях пониженных температур реакция прямого восстановления может иметь вид:
2 МеО + С ↔ 2 Ме + СО 2.
Если в процессе восстановления оксида углеродом происходит образование карбида, то состав равновесной газовой фазы смещается в сторону меньшего содержания СО и понижается температура начала восстановления.
3. Восстановитель - металл Ме'', обладающий более высоким химическим сродством к кислороду, чем металл Ме' восстанавливаемого оксида.
Ме'О + Ме'' ↔ Ме' + Ме''О.
Для этой реакции ∆G° = ½ (∆G°Ме''О - ∆G°Ме'О).
Восстановление будет протекать, если 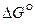 <0, т.е.
<0, т.е. 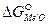 >
> 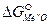 .
.
Система будет находиться в равновесии, если 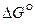 =0;
=0; 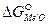 =
= 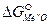 .
.
Следовательно, полнота завершения реакции восстановления оксида металлом будет тем большей, чем больше разница в величине приращения изобарного потенциала 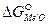 для образующегося и восстанавливаемого оксидов.
для образующегося и восстанавливаемого оксидов.
Большое значение в протекании процессов восстановления оксидов имеют разнообразные кинетические факторы.
ЗАКОНОМЕРНОСТИ ВЗАИМОДЕЙСТВИЯ МЕТАЛЛИЧЕСКИХ И ШЛАКОВЫХ РАСПЛАВОВ
В процессах черной металлургии участвуют две несмешивающиеся жидкие фазы с различным удельным весом: металл – расплав железа, содержащий другие элементы, и шлак – расплав оксидов и солей.
Взаимодействие между этими фазами имеют первостепенное значение, но изучение процессов с участием расплавов весьма затруднительно, так как они протекают при высоких температурах.
Для изучения процессов с участием расплавов важно знать их строение, то есть природу частиц, образующих жидкость и энергию их взаимодействия.
 2015-01-30
2015-01-30 3974
3974
