Атомные s-орбитали имеются на всех энергетических уровнях, атомные р-орбитали – на всех уровнях, кроме первого. На третьем и последующих энергетических уровнях к одной s-АО и трем р-АО присоединяется пять атомных орбиталей, получивших название d-орбиталей, а на четвертом и последующих уровнях — еще семь атомных орбиталей, называемых f-орбиталями.
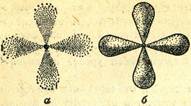
Граничные поверхности d- и f- АО отличаются большим разнообразием и очень сложны для наглядного изображения; пример одной из форм d-АО, так называемой четырехлепестковой розетки, показан на рис. 8.
|
Рис. 8.
Пять d-АО и семь f-АО одного энергетического уровня отличаются друг от друга не только по форме, но и по геометрическому расположению в пространстве, что передается различными значениями магнитного квантового числа, как и для трех р-АО. Каждая d-АО и f-АО может принять два электрона, следовательно, все d-АО одного энергетического уровня будут заполнены десятью, а все f-АО – четырнадцатью электронами.
Первый элемент, в атоме которого появляется d-электрон, – скандий, в атомах следующих элементов продолжается заполнение пяти Зd-АО электронами, которое заканчивается у цинка.
 2015-01-07
2015-01-07 679
679








