Стехиометрические уравнения показывают, в каких соотношениях реагенты вступают во взаимодействие. Они имеют вид:
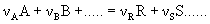 ,
,
где: 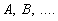 – исходные вещества;
– исходные вещества; 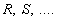 – продукты реакции;
– продукты реакции;
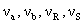 … - стехиометрические коэффициенты.
… - стехиометрические коэффициенты.
Химические превращения могут быть описаны одним или несколькими стехиометрическими уравнениями. В случае, когда имеет место несколько стехиометрических уравнений, стехиометрический коэффициент i -го вещества, j -го уравнения, можно обозначить, как 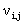 и систему уравнений можно представить в виде:
и систему уравнений можно представить в виде:
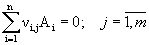 , где n – число реагентов, m – число уравнений,
, где n – число реагентов, m – число уравнений, 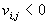 – для исходных реагентов,
– для исходных реагентов, 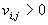 – для продуктов,
– для продуктов, 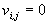 – для i-го вещества, не входящего в j-ое уравнение.
– для i-го вещества, не входящего в j-ое уравнение.
Совокупность стехиометрических уравнений, однозначно и полно описывающих процесс, называют базисной системой стехиометрических уравнений. Так как со стехиометрическими уравнениями можно делать линейные преобразования (складывать уравнения, переносить члены справа налево и наоборот и т.д.), то возникают трудности при определении базисной системы уравнений, например: процесс получения водорода из природного газа можно записать двумя уравнениями:
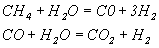 ,
,
но можно эти уравнения сложить и тогда:
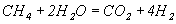 .
.
Для расчета данного процесса не достаточно последнего уравнения, хотя оно и является суммой предыдущих. Таким образом, базисная система линейно-независимых стехиометрических уравнений, однозначно описывающих процесс, должна включать все участвующие в химическом превращение вещества и не должна включать ни одного уравнения, которое может быть получено линейными преобразованиями других.
В большинстве случаев необходимое число стехиометрических уравнений можно определить по формуле: У=В-Э, где У - число независимых уравнений, В - число веществ (реагентов), Э - число химических элементов из которых состоят реагенты. Так для конверсии метана В=5 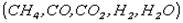 ; Э=3
; Э=3 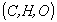 , откуда У=2. Базисная система включает два уравнения. Для отдельных обменных процессов формула имеет вид: У=В-Э+1.
, откуда У=2. Базисная система включает два уравнения. Для отдельных обменных процессов формула имеет вид: У=В-Э+1.
Основные виды технологических расчетов, которые могут быть выполнены только на основе стехиометрических зависимостей:
1. расчет материальных (массовых) балансов процесса;
2. расчет многих технологических показателей (степень превращения, селективность, и пр.);
3. расчет скорости превращения различных веществ в данных условиях.
Знание стехиометрических уравнений позволяет установить: как соотносятся между собой степени превращения, рассчитанные по разным веществам. Так для реакции вида:
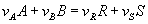
по определению:
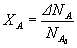 ;
; 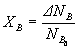 .
.
Если исходные вещества взяты в стехиометрическом соотношении, то степени превращения по всем исходным реагентам равны, т.е. 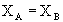 . А если какое-то вещество взято в избытке (например, В) по сравнению со стехиометрическим количеством в n раз, то степень превращения будет в n раз меньше, чем степень превращения другого вещества:
. А если какое-то вещество взято в избытке (например, В) по сравнению со стехиометрическим количеством в n раз, то степень превращения будет в n раз меньше, чем степень превращения другого вещества: 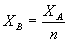 .
.
Стехиометрические закономерности позволяют получить более удобные для практического расчета выражения для выхода продукта и селективности. Для реакции вида:
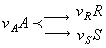
выход по продукту R будет равен:
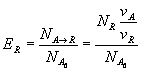 ,
,
для селективности S:
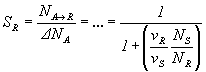 .
.
 2014-09-02
2014-09-02 935
935








