С помощью рис. 1 находим, что NaOH относится к классу оснований, а AlCl 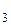 – к классу солей, между соединениями этих классов возможна реакция обмена:
– к классу солей, между соединениями этих классов возможна реакция обмена:
AlCl3 + 3NaOH = Al(OH)3¯ + 3NaCl
Al3+ + 3Cl– + 3Na+ + 3OH– = Al(OH)3¯ + 3Na+ + 3Cl–
Al3+ + 3OH– = Al(OH)3¯
Гидроксид алюминия относится к амфолитам. При взаимодействии гидроксида алюминия с избытком гидроксида натрия Al(OH)3 проявляет кислотные свойства:
Al(OH)3¯ + NaOH = Na[Al(OH)4]
Al(OH)3¯ + Na+ + OH– Á Na+ + [Al(OH)4] –
Al(OH)3¯ + OH– Á [Al(OH)4] –
При взаимодействии гидроксида алюминия с кислотой проявляются его свойства как основания:
Al(OH)3¯ + 3HNO3 = Al(NO3)3 + 3H2O
Al(OH)3¯ + 3H+ + 3NO–3 = Al3+ + 3NO–3 + 3H2O
Al(OH)3¯ + 3H+ = Al3+ + 3H2O
Пример 4. Составьте уравнения реакций, которые позволяют осуществить следующие превращения. Пользуясь табл. 1.1, для каждого превращения обоснуйте выбор реагента и укажите условия необратимости реакции. Запишите соответствующие молекулярные и ионные уравнения.
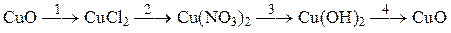
 2015-02-27
2015-02-27 541
541








