1 Взаимодействие простых веществ:
2Fe + 3Cl2 = 2FeCl3
2 Взаимодействие металлов, находящихся в ряду напряжений левее водорода, с водными растворами кислот:
Zn + 2HCl = ZnCl2 + H2
3 Взаимодействие более активных металлов с растворами или расплавами солей менее активных металлов:
Fe + CuSO4 = FeSO4 + Cu
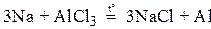
4 Взаимодействие металлов, проявляющих амфотерные свойства, с растворами щелочей:
Zn + 2H2O + 2NaOH = Na2[Zn(OH)4] + H2
5 Взаимодействие кислотного оксида с основаниями:
CO2 + NaOH = NaHCO3 или
CO2 + 2NaOH = Na2CO3 + H2O
6 Взаимодействие оснớвного оксида с кислотами:
FeO + H2SO4 = FeSO4 + H2O
7 Взаимодействие кислотных и основных оксидов:
CO2+ BaO = BaCO3
8 Взаимодействие некоторых амфотерных оксидов с кислотными оксидами:
ZnO + N2O5 = Zn(NO3)2
9 Взаимодействие амфотерных и оснớвных оксидов (сплавление):
Al2O3 + MgO = Mg(AlO2)2 (при 1600 ˚С)
10 Взаимодействие кислот и оснований (реакция нейтрализации):
2NaOH + H2SO4 = Na2SO4 + 2H2O
H3PO4 + NH4OH = NH4H2PO4 + H2O
11 Взаимодействие соли с кислотой, в результате которого образуется нерастворимое или летучее вещество:
AgNO3 + HCl = AgCl¯ + HNO3
FeS + H2SO4 = H2S↑ + FeSO4
12 Взаимодействие растворимой соли со щёлочью, в результате которого образуется нерастворимое соединение:
MgCl2 + 2KOH = Mg(OH)2¯ + 2KCl
Na2CO3 + Ca(OH)2 = CaCO3↓ + 2NaOH
13 Взаимодействие растворимых солей друг с другом, в результате которого образуется нерастворимое соединение:
3AgNO3 + Na3PO4 = Ag3PO4¯ + 3NaNO3
14 Вытеснение более активным неметаллом менее активного из его солей:
Br2 + 2KI = I2 + 2KBr
15 Окисление (или восстановление) некоторых солей:
2FeCl2 + Cl2 = 2FeCl3
Na2SO3 + O2 = Na2SO4
2FeCl3 + Cu = 2FeCl2 + CuCl2
 2015-02-27
2015-02-27 475
475








