100 г раствора содержит 1 г, а 1 л – 10 г НСООН, поэтому молярная концентрация кислоты составляет:
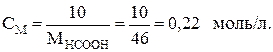
Из формулы (7.28) следует, что:
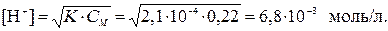
Вычислим рН:
рН = –lg[H+] = –lg6,8∙10–3 = 2,2.
Задачи
151 – 156 Вычислить массовую долю (%), молярную, моляльную и нормальную концентрацию указанных растворов (см. таблицу), если известны плотность раствора, масса растворенного вещества и объем воды.
| № задачи | Вещество | Масса раство- ренного вещества, г | Объем воды, мл | Плот- ность раствора, г/мл | Ответ | |||
| Концентрация раствора | ||||||||
| Нор- маль-ная | Мас- совая доля, % | Моляр- ная | Моляль- ная | |||||
| Н2SO4 | 10,45 | 39,55 | 1,15 | 4,9 | 20,9 | 2,45 | 2,70 | |
| FeSO4 | 5,0 | 20,0 | 1,21 | 3,18 | 20,0 | 1,59 | 1,64 | |
| HNO3 | 1,1 | 18,9 | 1,08 | 0,94 | 5,5 | 0,94 | 0,92 | |
| CuSO4 | 1,2 | 13,8 | 1,084 | 1,09 | 8,0 | 0,54 | 0,55 | |
| NaOH | 79,8 | 186,2 | 1,33 | 9,97 | 30,0 | 9,97 | 10,7 | |
| HCl | 36,2 | 63,8 | 1,18 | 11,70 | 36,2 | 11,70 | 15,45 |
157 – 161 Вычислить объём V′ (мл) разбавленного раствора, полученного добавлением воды к 250 мл концентрированного раствора (см. таблицу). Рассчитать молярную долю растворенного вещества в разбавленном растворе.
| № задачи | Растворенное вещество | Концентрированный раствор | Разбавленный раствор | Ответ | |||
| V, мл | ω,% | ρ г/мл | ω,% | ρ, г/мл | |||
| HClO4 | 18,0 | 1,176 | 10,0 | 1,095 | 483 мл; 0,07 | ||
| HNO3 | 16,0 | 1,171 | 4,0 | 1,039 | 1115 мл; 0,012 | ||
| NaOH | 14,0 | 1,118 | 8,0 | 1,065 | 460 мл; 0,038 | ||
| KOH | 20,0 | 1,214 | 6,0 | 1,058 | 963 мл; 0,02 | ||
| H3PO4 | 24,0 | 1,206 | 2,0 | 1,013 | 3618 мл; 0,001 |
162 – 167 Рассчитать массовую долю (ω, %) растворенного вещества в растворе, приготовленном смешением 100 мл разбавленного раствора и 10 мл концентрированного раствора указанного вещества (см. таблицу).
| № задачи | Растворенное вещество | Разбавленный раствор | Концентрированный раствор | Ответ | ||
| СМ, моль/л | ρ, г/мл | ω, % | ρ, г/мл | |||
| CH3COOH | 1,0 | 1,007 | 1,064 | 11,1 | ||
| HNO3 | 0,95 | 1,030 | 1,310 | 10,8 | ||
| H2SO4 | 1,07 | 1,065 | 1,806 | 22,3 | ||
| KOH | 1,06 | 1,050 | 1,186 | 7,1 | ||
| BaCl2 | 0,2 | 1,034 | 1,253 | 14,4 | ||
| AlCl3 | 0,31 | 1,029 | 1,272 | 6,8 |
168 – 172 Вычислите, до какого объема (л) необходимо выпарить 2,5 л разбавленного раствора, чтобы приготовить концентрированный раствор с молярной концентрацией 1,2 моль/л (см. таблицу).
| № задачи | Растворенное вещество | Разбавленный раствор | Ответ | |
| w, % | ρ, г/мл | |||
| NaOH | 1,5 | 1,015 | 0,79 | |
| KOH | 1,3 | 1,010 | 0,49 | |
| Na2SO4 | 3,0 | 1,026 | 0,45 | |
| Ca(NO3)2 | 6,0 | 1,045 | 0,80 | |
| MnCl2 | 1,0 | 1,007 | 0,17 |
173 Для нейтрализации 20 мл 0,1 н раствора кислоты потребовалось 8 мл раствора NaOH. Сколько граммов NaOH содержит 1 л этого раствора?
Ответ: 10 г.
174 На нейтрализацию 20 мл раствора, содержащего в 1 л 12 г NaOH, израсходовано 24 мл раствора кислоты. Определить нормальность раствора кислоты.
Ответ: 0,25 н.
175 Какой объем 0,2 н раствора щелочи NaOH потребуется для осаждения в виде Fe(OH)3 всего железа, содержащегося в 100 мл 0,5 н раствора FeCl3? Какая масса Fe(OH)3 выпадает в осадок?
Ответ: 0,25л; 1,78 г.
176 Сколько граммов СаСО3 выпадает в осадок, если к 400 мл 0,5 н раствора СaCl2 прибавить избыток раствора соды?
Ответ: 10 г.
177 Давление пара воды при 100 ˚С равно 1,013 ∙ 105 Па. Вычислите давление пара над 4 %-ным раствором мочевины СО(NH2)2 при этой температуре.
Ответ: 1∙105 Па.
178 – 179 По данным, приведенным в таблице для разбавленных растворов неэлектролитов, вычислить указанные в ней искомые величины, обозначенные знаком «?».
| № задачи | Р 0Н2О, Па | Р раствора, Па | Масса неэлектролита, г | Масса воды, г | Молярная масса неэлектролита, г/моль | Ответ |
| 3,168∙102 | 3,121∙103 | ? | 60 г/моль | |||
| 25∙103 | ? | 13,7 (С12Н22О11) | – | 23∙103 Па |
180 Что такое эбуллиоскопическая и криоскопическая константы растворителя? Вычислите криоскопическую константу бензола, если при растворении 0,0125 вещества в 125 г бензола температура кристаллизации понижается на 0,512 ˚С.
Ответ: 5,12 ˚С.
181 Температура кристаллизации уксусной кислоты 16,65 ˚С, а криоскопическая константа равна 3,9. Вычислить температуру кристаллизации раствора, содержащего 0,1 моля растворенного вещества в 125 г уксусной кислоты.
Ответ: 13,53 ˚С.
182 – 183 Вычислить молярную массу неэлектролита (г/моль), используя данные таблицы:
| № задачи | Масса неэлектролита, г | Масса растворителя, г | Для раствора | Для растворителя | Ответ | |||
| t зам, ˚С | t кип, ˚С | t кип, ˚С | К | Е | ||||
| 0,512 | – | 46,67 | 46,2 | – | 2,36 | |||
| 5,18 | –1,39 | – | – | 1,86 | – |
184 – 187 По данным, приведенным в таблице для разбавленных водных растворов неэлектролитов, вычислить указанные там же искомые величины, обозначенные знаком «?».
| № задачи | Растворенное вещество | Концен- трация, % | t зам, ˚С | t кип, ˚С | К | Е | Ответ |
| С2Н6О2 | ? | ? | 1,86 | 0,52 | –3,33 ˚С; 100,93 ˚С | ||
| СО(NH2)2 | ? | –0,93 | – | 1,86 | – | 3 % | |
| С6Н12О6 | –1,15 | 100,32 | ? | ? | 0,518; 1,86 | ||
| С3Н7ОН | ? | – | 102,17 | – | 0,25 | 20 % |
188 Вычислить давление пара 10 %-го раствора Ba(NO3)2 при 28 ˚С. Давление пара воды при той же температуре составляет 37,8∙102 Па. Кажущая степень диссоциации соли 0,2.
Ответ: 37,18∙102 Па.
189 Вычислить рН и рОН 0,01 н раствора уксусной кислоты, степень диссоциации которой в этом растворе равна 4,2 %.
Ответ:3,38; 10,62.
190 Могут ли рН и рОН быть равными нулю? Меньше нуля? Чему равны рН и рОН раствора, концентрация ионов водорода в котором равна 10–4 моль/л?
Ответ: 4; 10.
191 – 194 По данным, приведенным в таблице для разбавленных водных растворов электролитов, вычислите там же искомые величины, обозначенные знаком «?».
| № задачи | Электро-лит | Масса элек-троли-та, г | Объ-ем во-ды, мл | Кон-цен-тра-ция, % | t зам, ˚С | t кип, ˚С | α | i | K | E | Ответ |
| KNO3 | 9,09 | – | – | 100,8 | ? | ? | – | 0,52 | 1,7; 0,71 | ||
| Na2SO4 | 0,53 | – | – | – | ? | – | 1,86 | – | 0,9 | ||
| KCl | – | – | 3,2 | 0,13 | ? | 0,68 | – | – | 0,52 | 100,4 | |
| BaCl2 | – | – | 3,0 | – | 100,28 | ? | ? | – | 0,52 | 2,54; 0,77 |
195 Константа диссоциации хлорноватистой кислоты равна 3,0∙10–8 при 25 ˚С. Чему равна степень диссоциации HClO в 0,1 н растворе?
Ответ: 5,5∙10–4.
196 Вычислить концентрацию ионов Н+ и ОН– в растворе, водородный показатель которого равен 4,3.
Ответ: 5∙10–5 моль/л; 2∙10–10 моль/л.
197 Определить молярную концентрацию раствора серной кислоты, если рН равен 2,2.
198–200 Вычислить рН раствора кислоты при α = 1, если для обозначенного известны из таблицы следующие данные:
| № задачи | Кислота | Объем кислоты, мл | Плотность, г/мл | Концен- трация, % | Объем раствора, л | Ответ |
| H2SO4 | 1,84 | 1,62 | ||||
| HCl | 1,015 | 3,12 | – | 0,06 | ||
| HNO3 | 1,43 | 1,79 |
 2015-02-27
2015-02-27 1982
1982
