Вязкость жидкости можно определять по скорости истечения жидкости через капилляр. В цилиндрических капиллярах для ламинарного протекания жидкости существует зависимость, установленная Пуазелем:
V = 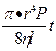
V – объем жидкости, вытекающий из капилляра, см3;
r – радиус капилляра, см;
P – сила, под действием которой движется жидкость, дина;
t – время протекания, с;
l – длина капилляра, см
Отсюда:
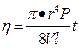 и t =
и t = 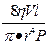
Определение абсолютной величины вязкости по формуле Пуазейля связано с рядом экспериментальных трудностей, поэтому на практике находят относительную вязкость.
Относительную вязкость можно определить по времени протекания одинаковых объемов испытуемой и стандартной жидкостей через один и тот же капилляр. В качестве стандартной жидкости для водных растворов обычно принимают воду.
Метод измерения относительной вязкости основан на том, что при соблюдении указанных выше условий V, r, l являются постоянными величинами, т. е.
k = 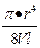
где k – постоянная величина. Тогда:
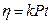
Определив время истечения некоторого объема воды (в секундах) и такого же объема исследуемой жидкости и зная ее плотность (ρН2О=1 г/см3), определяют относительную вязкость по формуле:
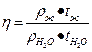
Прибором для измерения относительной вязкости может служить капиллярный вискозиметр. Простейший из них – вискозиметр Оствальда (рис.) представляет собой две сообщающиеся стеклянные трубки 1 и 2. Трубка 1 имеет расширение 3, переходящее в капилляр 4, через трубку 2 исследуемая жидкость протекает под влиянием собственной тяжести в трубку 1. Выше и ниже расширения 3 на трубке 1 имеются метки 5 и 6. Объем расширенной части трубки обычно равен 3-4 мл.
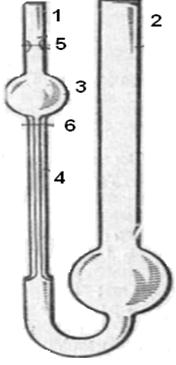
Рис. Капиллярный вискозиметр.
Перед работой вискозиметр промывают хромовой смесью и дистиллированной водой, а затем просушивают в сушильном шкафу. Вискозиметр укрепляют вертикально и наливают пипеткой несколько миллилитров исследуемой жидкости в трубку 2. Затем жидкость засасывают вверх по узкой трубке точно до метки 5. Время необходимое для понижения уровня жидкости от метки 5 до метки 6, измеряют секундомером.
В чистый сухой вискозиметр наливают через трубку 2 воду в объеме 15-20 мл. Присоединяют к колену 1 резиновую грушу для засасывания жидкости. Жидкость должна быть выше метки 5 примерно на 1 см. Затем жидкости дают свободно вытекать, отмечая секундомером время, за которое уровень воды опускается по капилляру от верхней метки 5 до нижней 6. Делают несколько отсчетов и берут среднее значение 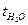 .
.
Воду сливают, выдавливая последние капли из капилляра с помощью груши, вискозиметр прополаскивают 2-3 раза исследуемой жидкостью (раствором), затем наполняют им трубку 2 в том же объеме, что и водой (15-20 мл). Измеряют время истечения жидкости 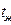 .
.
Полученные средние значения 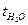 и
и 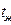 подставляют в формулу:
подставляют в формулу:
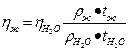
При небольшой разности между плотностями исследуемой и эталонной жидкостей формула упрощается:
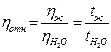
Опыт 1. Измерение вязкостей золей гидроксида железа (III) и желатины. При постоянной температуре определяют повыше указанному методу относительную вязкость золей. Сравнивают полученные результаты.
Опыт 2. Влияние концентрации раствора на вязкость. Из горячего 1% золя желатина готовят следующие растворы:
Таблица 21
| Состав | № раствора | |||
| Золь желатина, мл | ||||
| Вода, мл |
Охлаждают приготовленные растворы до температуры опыта. Измеряют вязкость полученных растворов. Вычерчивают кривую изменения вязкости с изменением концентрации.
Опыт 3. Влияние температуры на вязкость. Измеряют время истечения 0,5%- ного золя желатина поместив вискозиметр в воду при 20, 40 и 60°С. Вычерчивают кривую изменения вязкости в зависимости от температуры.
Опыт 4. Влияние солей на вязкость. В три пробирки наливают по 5 мл 1% золя желатина, затем в первую пробирку приливают 5 мл 1 н раствора KI, во вторую 5 мл 1 н раствора K2SO4, а в третью 5 мл дистиллированной воды.
Тщательно взбалтывают содержимое пробирок и оставляют в покое приблизительно на час. После этого определяют вязкость.
Полученные результаты заносят в таблицу и делают выводы о влиянии анионов на вязкость золя.
Таблица 22
Результаты опыта.
| Раствор | Вязкость |
| 1%-ный ра-р желатина | |
| 1%-ный ра-р желатина + KI | |
| 1%-ный ра-р желатина + K2SO4 |
Контрольные вопросы по теме: «Коллоидные растворы».
1. Классификация дисперсных систем.
2. Коллоидно-дисперсные системы (золи) в природе и технике.
3. Оптические и кинетические свойства золей.
3. Электрокинетические явления. Электрокинетический потенциал.
4. Строение коллоидных частиц.
5. Методы получения золей.
6. Кинетическая и агрегативная устойчивость.
7. Коллоиды гидрофобные и гидрофильные?
 2015-02-04
2015-02-04 1553
1553








