По широте использования занимают второе место после β-лактамных антибиотиков. Они высокоэффективны в случае пневмонии, коклюша, гонореи, тифа.
В 1948 г. Даггером был получен ферментацией первый тетрациклиновый антибиотик (хлортетрациклин).
В 1952 г. был осуществлен полный синтез и расшифрована структура.
Путём ферментации можно выделить 6 различных тетрациклинов. Общая формула тетрациклинов
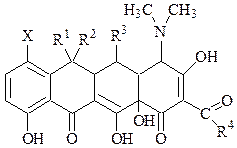
тетрациклин-основание имеет вид:Х=Н, R1=CH3, R2=OH, R3=H, R4=NH2.
хлортетрациклин: Х=Cl, R1=CH3, R2=OH, R3=H, R4=NH2
бромтетрациклин: Х=Br, R1=H, R2=H, R3=H, R4=NH2
окситетрациклин:: Х=H, R1=CH3, R2=OH, R3=OH, R4=NH2
Схема 87
В отличие от β-лактамов поиск синтетических аналогов тетрациклина оказался малоплодотворным. В настоящее время используются 3 из них.
Небольшими структурными изменениями удалось получить моноциклины.
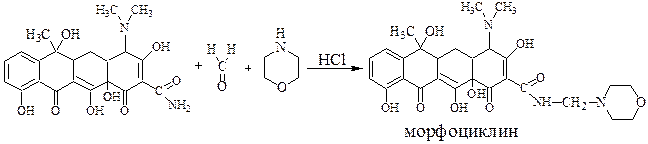
Схема 88
Существует также переход:
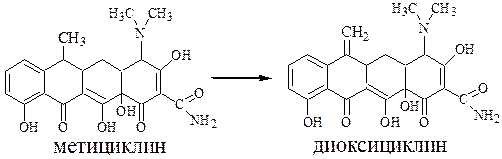
Схема 89
Тетрациклины относятся к очень токсичным антибиотикам, в ряде случаев получение их полусинтетических аналогов приводило к усилению токсичности, получают его исключительно ферментацией. Тетрациклины очень сильно склонны к кумуляции в организме (в печени, почках, сердце, костях), образуют очень прочные комплексы со многими металлами, в частности с кальцием, магнием, железом, кобальтом (поэтому, кстати, тетрациклины нельзя запивать молоком – связывание с кальцием).
Тетрациклины обладают широким спектром действия (активны против Г+ и Г–-бактерий), механизм антибиотического действия до настоящего времени малоизучен, хотя в 1950 г. было показано, что хлортетрациклин является специфическим ингибитором синтеза белка бактерий. В настоящее время известно, что тетрациклины в присутствии ионов К+ и Мg2+ образуют прочные комплексы с 70 рибосомальными единицами, в результате чего и нарушается синтез белка.
 2015-02-04
2015-02-04 1479
1479








