Как уже отмечалось, поведение реальных газов довольно хорошо описывается уравнением (5)
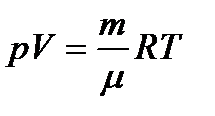
только при не слишком высоких давлениях и достаточно высоких температурах. С повышением давления и уменьшением температуры наблюдаются значительные отступления от уравнения. Во втором столбце таблицы 1 приведены значения произведения pV для массы азота, занимающей при нормальных условиях объем, равный одному литру. Указанные значения даны для различных давлений и одной и той же температуры 0°С. В соответствии с уравнением (5) произведение pV при неизменной температуре должно оставаться постоянным. В действительности, как видно из таблицы, при давлениях порядка 200 ат наблюдаются заметные отклонения, которые, непрерывно возрастая с увеличением давления, достигают при 1000 ат более 100%. Эти отклонения не представляются удивительными, поскольку в модели идеального газа не учитываются размеры молекул и их взаимодействие друг с другом на расстоянии. Вместе с тем при повышении давления возрастает плотность газа, что приводит к уменьшению среднего расстояния между молекулами; поэтому объем молекул и взаимодействие между ними начинают играть существенную роль.
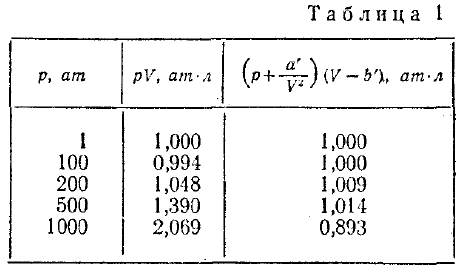
 2015-02-15
2015-02-15 1282
1282








