Так называется процесс, проводимый при постоянной температуре газа (Т = const). При изотермическом процессе выполняется закон Бойля-Мариотта
pV = const.
Для двух состояний это уравнение запишется в виде
p1V1 = p2V2.
На pV -диаграмме этот процесс изображается гиперболой(рис. 38).
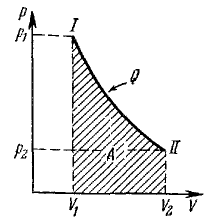
Рис. 38. pV-диаграмма изотермического процесса
Поскольку внутренняя энергия идеального газа зависит только от его температуры, то при изотермическом расширении U = const и Δ U = 0. Следовательно, согласно первому началу термодинамики
Q = A. (107)
Подводимое к газу при изотермическом расширении тепло целиком превращается в работу расширения.
Работа одного моля идеального газа при изотермическом расширении равна
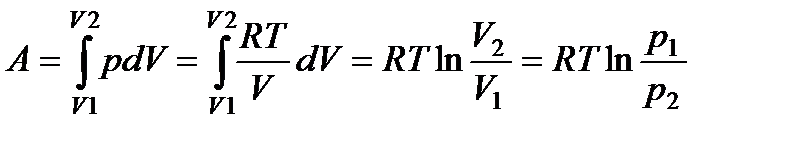 . (108)
. (108)
Теплоемкость газа при T = const:
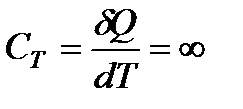 .
.
Это означает, что понятие теплоемкости при изотермическом процессе смысла не имеет.
Бесконечная теплоемкость не является физическим абсурдом. Она означает, что подводимое к газу тепло не приводит к изменению его температуры в силу того, что все оно идет на совершение газом внешней работы. При изотермическом процессе увеличение внутренней энергиигаза за счет притока тепла целиком компенсируется уменьшением внутренней энергии вследствие произведенной газом работы расширения. Таким образом, внутренняя энергия газа остается неизменной.
 2015-02-15
2015-02-15 1712
1712
