Идеальный газ – модель реального газа, которая удовлетворяет следующим требованиям:
· расстояние между молекулами гораздо больше их размеров (молекулы можно считать материальными точками);
· силами взаимодействия, кроме моментов соударения, можно пренебречь (потенциальная энергия взаимодействия молекул по сравнению с кинетической энергией хаотического движения пренебрежимо мала);
· столкновение молекул друг с другом и со стенками абсолютно упругое;
· движение каждой молекулы подчиняется классическим законам динамики.
· реальный разреженный газ приблизительно ведет себя как идеальный газ.
Изопроцессы – равновесные процессы, в которых один из основных параметров сохраняется.
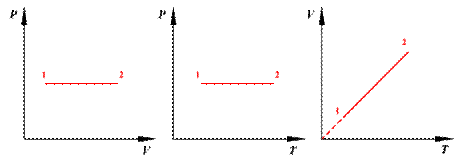
Изобарный процесс (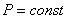 ) Для изобарного процесса в идеальном газе справедлив закон Гей-Люссака: при постоянном давлении объем данной массы газа прямо пропорционален его термодинамической температуре:
) Для изобарного процесса в идеальном газе справедлив закон Гей-Люссака: при постоянном давлении объем данной массы газа прямо пропорционален его термодинамической температуре:
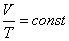 или
или 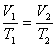 .
.
Работа газа при изобарном расширении:
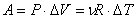 .
.
Изменение внутренней энергии:
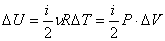
Количество полученного тепла:
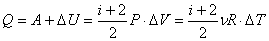 .
.
Молярная теплоемкость при изобарном процессе:
 .
.
Изохорный процесс (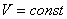 ) Изохорный процесс в идеальном газе описывается законом Шарля: при постоянном объеме давление данной массы газа прямо пропорционально его термодинамической температуре:
) Изохорный процесс в идеальном газе описывается законом Шарля: при постоянном объеме давление данной массы газа прямо пропорционально его термодинамической температуре:
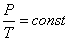 или
или 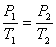 .
.
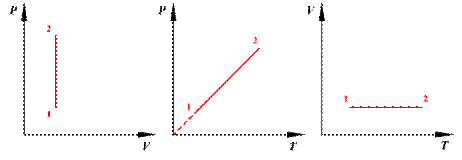
Работа газа при изохорном процессе равна нулю: 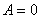 .
.
Все полученное тепло идет на изменение внутренней энергии согласно первому закону термодинамики:
 .
.
Молярная теплоемкость при изохорном процессе:
 .
.
Изотермический процесс (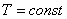 ) Изотермический процесс в идеальном газе подчиняется закону Бойля - Мариотта: для данной массы газа при неизменной температуре произведение значений давления и объема есть величина постоянная:
) Изотермический процесс в идеальном газе подчиняется закону Бойля - Мариотта: для данной массы газа при неизменной температуре произведение значений давления и объема есть величина постоянная:
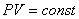 или
или 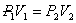 .
.
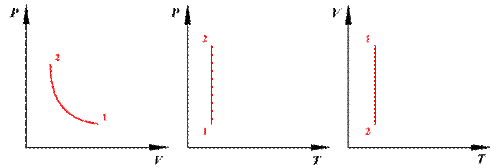
Работа газа при изотермическом расширении:
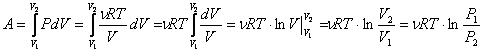 .
.
Изменение внутренней энергии при изотермическом процессе равно нулю:
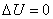 .
.
Все полученное тепло идет на совершение работы в соответствии с первым началом термодинамики:
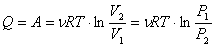 .
.
Адиабатный процесс – процесс, при котором отсутствует теплообмен между системой и окружающей средой.
Из первого начала термодинамики следует, что работа газа при адиабатном процессе совершается за счет его внутренней энергии:
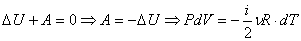 (6.1)
(6.1)
С другой стороны, из уравнения Клапейрона-Менделеева следует:
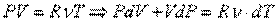 (6.2).
(6.2).
Разделим уравнение (2) на уравнение (1):
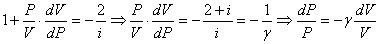 ,
,
где показатель адиабаты: 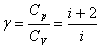 .
.
Проинтегрируем полученное уравнение:
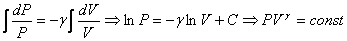 .
.
Таким образом, при адиабатном процессе  или
или 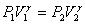 – уравнение Пуассона. С учетом уравнения Клапейрона-Менделеева (
– уравнение Пуассона. С учетом уравнения Клапейрона-Менделеева (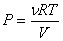 ,
,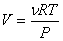 ) уравнение Пуассона может быть представлено в виде:
) уравнение Пуассона может быть представлено в виде:
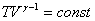 или
или 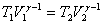 ;
; 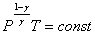 или
или  .
.
График адиабатного процесса — более крутая кривая, чем гипербола при изотермическом процессе. Это следует из выражения производной 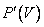 , полученной из уравнения Пуассона.
, полученной из уравнения Пуассона.

Работа газа при адиабатном процессе равна убыли внутренней энергии:
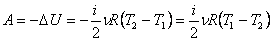 .
.
Политропный процесс.
Рассмотренные изобарный, изохорный, изотермический и адиабатический процессы имеют общую особенность – они происходят при постоянной теплоемкости.
В первых двух процессах теплоемкости соответственно равны СV и Сp, в изотермическом процессе (dT = 0) теплоемкость равна ±∞, в адиабатическом (δQ = 0) теплоемкость равна нулю.
Процесс, в котором теплоемкость остается неизменной, называется политропным.
Исходя из первого начала термодинамики при условии постоянства теплоемкости (C = const) можно вывести уравнение политропы:
 (6.3)
(6.3)
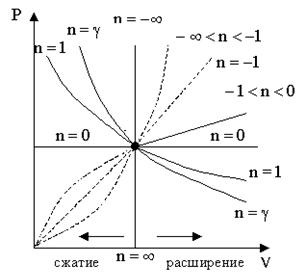
где n = (С – Сp)/(С – СV) – показатель политропы.
При С = 0, n = γ, из (3) получается уравнение адиабаты; при С = 0, n = 1 – уравнение изотермы; при С = Сp, n = 0 – уравнение изобары, при С = СV, n = ±∞ – уравнение изохоры. Таким образом, все рассмотренные процессы являются частными случаями политропного процесса.
Теплота в политропном процессе: 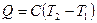 ,
,
где С – теплоемкость политропного процесса.
Процессы расширения
1.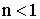 :
: 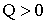 (тепло подводится),
(тепло подводится), 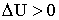 .
.
2.  :
: 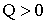 ,
, 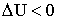 .
.
3. 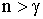 :
: 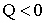 (тепло отводится),
(тепло отводится), 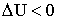 .
.
Процессы сжатия
1. 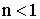 :
: 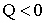 ,
, 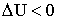 .
.
2.  :
: 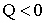 ,
, 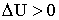 .
.
3. 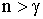 :
: 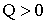 ,
, 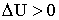 .
.
 2014-02-24
2014-02-24 1387
1387
