Посмотрим теперь, как ведет себя энтропия при необратимых процессах. Пусть система переходит из равновесного состояния 1 в равновесное состояние 2 необратимым образом (рис. 42).
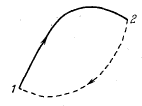
Рис. 42. Вычисление энтропии при необратимом процессе 1 –> 2
Необратимость перехода означает, что промежуточные состояния неравновесны. Вернем систему в первоначальное состояние каким-нибудь обратимым путем, например путем, показанным на рис. 42 пунктирной линией. Получившийся круговой процесс необратим, потому что одна его часть необратима. Поэтому для него справедливо неравенство Клаузиуса
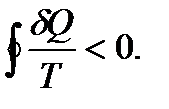
В нашем случае циклический интеграл можно представить в виде суммы двух интегралов:
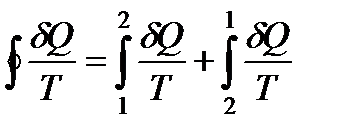 .
.
Поскольку второй интеграл описывает обратимый процесс, то он равен разности энтропий 1-го и 2-го состояний:
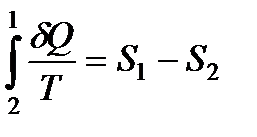 .
.
Следовательно:
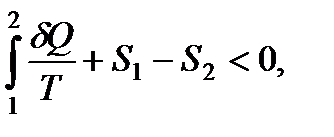 или
или 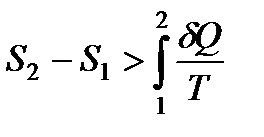 .
.
Если система замкнута, то δQ = 0, и S2 – S1 >0, или S2 > S1.
Мы получили, что энтропия замкнутой системы при необратимом процессе возрастает.
Объединяя выводы для обратимого и необратимого процессов, получаем закон возрастания энтропии:
 2015-02-15
2015-02-15 1097
1097
