1. Найдем среднюю молярную массу газовых смесей А и В: М (А) = М (В) = 18·2 =
= 36 г/моль. Эти смеси содержат в своем составе по два компонента в равных мольных соотношениях, а одним из компонентов смеси В, вызывающим помутнение известковой воды и не обесцвечивающим раствор перманганата калия, является углекислый газ (молярная масса M I = 44 г/моль):
CO2 + Ca(OH)2 ® CaCO3¯ + H2O (5)
Молярная масса МII второго компонента смеси В: 0,5·44 + 0,5· МII = 36 Þ МII = 28 г/моль.
Один из компонентов смеси А взаимодействует с оксидом иода (V). Эта реакция используется в аналитической химии для количественного определения оксида углерода (II), который окисляется до углекислого газа:
5CO + I2O5 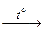 5CO2 + I2. (4)
5CO2 + I2. (4)
Таким образом, смесь А состоит из угарного газа (молярная масса 28 г/моль) и газа с молярной массой 44 г/моль (N2O, CO2, C3H8), а смесь В – из углекислого газа и газа с молекулярной массой 28 г/моль (N2, CO, C2H4, В2Н6).
Уменьшение плотности смесей А и В (до 14 × 2 = 28 г/моль) при пропускании над раскаленным углем говорит о наличии в их составе газов, проявляющих окислительные свойства в этой реакции. Такими газами могут быть N2O и СО2. Следовательно, смесь А – N2O + СО, смесь В – СО2 + N2.
N2O + C 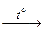 N2 + CO (3)
N2 + CO (3)
CO2 + C 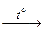 2CO (2)
2CO (2)
N2O + CO 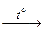 N2 + CO2 (1)
N2 + CO2 (1)
2. Структурные формулы молекул оксидов азота (I), углерода (II) и (IV), диазота:

3. Оксид азота (I) в лаборатории получают при термическом разложении нитрата аммония:
NH4NO3 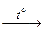 N2O + 2H2O.
N2O + 2H2O.
Для получения углекислого газа в лаборатории обычно используют взаимодействие карбонатов с минеральными кислотами, например:
CaCO3 + 2HCl ® CaCl2 + H2O + CO2.
Угарный газ в лаборатории можно получить при взаимодействии муравьиной или щавелевой кислоты с концентрированной серной кислотой (правда, в последнем случае образуется смесь угарного и углекислого газа, поэтому для получения угарного газа в чистом виде образовавшуюся смесь пропускают через раствор щелочи):
HCOOH 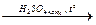 CO + H2O;
CO + H2O;
H2C2O4 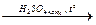 CO + CO2 + H2O.
CO + CO2 + H2O.
Молекулярный азот можно получить при нагревании раствора нитрита аммония:
NH4NO2 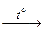 N2 + 2H2O (NH4Cl + NaNO2
N2 + 2H2O (NH4Cl + NaNO2 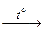 N2 + 2H2O + 2NaCl).
N2 + 2H2O + 2NaCl).
4. CO + NaOH 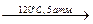 HCOONa (6)
HCOONa (6)
N2O + 2NaNH2 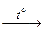 NaN3 + NaOH + NH3 (7)
NaN3 + NaOH + NH3 (7)
5. 3Mg + N2 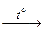 Mg3N2 (8)
Mg3N2 (8)
2Mg + CO2 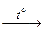 2MgO + C (9)
2MgO + C (9)
Система оценивания:
1. Составы смесей А и В 1,5 балла ´ 2 = 3 балла;
Уравнения реакций 1–5 1 балл ´ 5 = 5 баллов;
2. Структурные формулы CO, N2O, CO2, N2 1 балл ´ 4 = 4 балла;
3. Способы получения CO, N2O, CO2, N2 1 балл ´ 4 = 4 балла;
4. Уравнения реакций 6, 7 1 балл ´ 2 = 2 балла;
5. Уравнения реакций 8, 9 1 балл ´ 2 = 2 балла;
Итого 20 баллов.
 2015-04-12
2015-04-12 349
349








