Общая формула эфира СnH2n+2O. Метиловый и метилэтиловый эфиры при обычных условиях - газы. Все остальные простые эфиры - жидкости, которые кипят при температурах, значительно более низких, чем соответствующие спирты - это связано с отсутствием водородной связи между молекулами эфиров. Эфиры плохо растворимы в воде, их плотность <1, они обладают характерным неприятным запахом.
Хим.свойства. Взаимодействие с конц кислотами при низких температурах (обр оксониевые соли(диметилоксоний хлорид)),
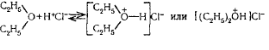
с конц кислотами при высоких Т (ацидолиз - обр спирт и галогеналкил),

реакция Шорыгина (взаимодействие с Na или К при нагревании)
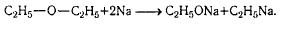
окисление (образуется гидроперекись).
СН3-СН2-О-СН2-СН3 + О2 → СН3-СН(О-О-Н)-О-СН2-СН3 – гидроперекись этилового эфира.
Получение. Реакция Вильямсона (взаимод CH3Cl+CH3ONa),
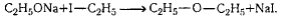
дегидратация спиртов (межмолекулярная).
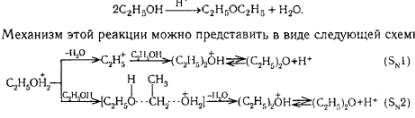
Применение. Этиловый эфир- растворитель, в медицине его употребляют для наркоза и усиления сердечной деятельности.
 2015-04-17
2015-04-17 1941
1941








