При взаимодействии с веществами, которые сами являются достаточно сильными нуклеофилами (амины), раскрытие цикла может происходить и без помощи электрофила:
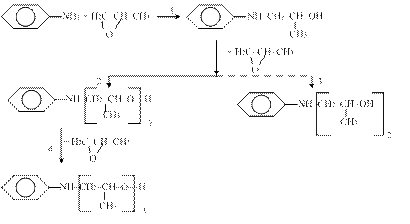
Некаталитическая реакция -протекает значительно медленнее (достаточная ее скорость протекания достигается при 180-220 ºС, в отличие от 100-150 ºС при нуклеофильном катализе).
В этих реакциях пропиленоксид берут в недостатке по отношению к другому компоненту, их мольное соотношение поддерживают от 1: (4-5) до (2-3):1. В этих случаях выделение тепла велико, и в отсутствии охлаждения неизбежен перегрев реакционной массы. Наиболее типичными реакторами для таких процессов являются КТА или колонка с выносным охлаждением. КТА должно работать под давлением, обеспечивающим нахождение смеси в жидком состоянии.
Спирты
Спиртами называют гидроксильные производные УВ. Спирты могут быть предельными и непредельными. Атомность спиртов определяется числом гидроксильных групп -ОН. Общая формула СnH2n+2О. В зависимости от того, при каком С атоме, первичном, вторичном или третичным, находится гидроксил, различают перв, втор, третич.
Спирты до С10 при обыкновенной температуре - жидкости, начиная с С11 и выше - твердые тела. Спирты С1-С2 смешиваются с водой во всех соотношениях и имеют характреный запах. По мере увеличения молекулярной массы растворимость жидких спиртов в воде уменьшается, и запах их становится неприятным. Твердые спирты лишены запаха и почти нерастворимы в воде. Жидкие спирты являются хорошими растворителями многих органических веществ. Темп кипения спиртов возрастает по мере увеличения их молекулярной массы. Спирты нормального строения кипят при более высокой температуре, чем спирты с разветвленной цепью.
Получение. Спирты получают:
- гидролизом (галогеналкилов при нагревании с водой),
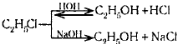
гидратацией (присоединение воды к алкенам),
СН2=СН2 + Н2О →Н+ или AL2O3 СН3-СН2-ОН
восстановлением альдегидов, кетонов, сложных эфиров (Ni, Co, Cu,Pt, Pd).
Хим.свойства спиртов обусловлены присутствием реакционноспособной гидроксильной группы. Реакции с участием этой группы проводят с разрывом связи О-Н или С-О.
Кислотные свойства:
- реакции с щелочными Ме,
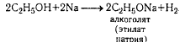
- реакция этерификация - с карбоновыми кислотами),
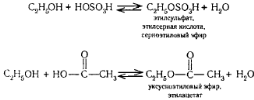
реакции нуклеофильного замещения (HCl, PCl3,PCl5, SOCl2),
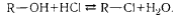
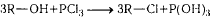
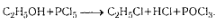

реакции отщепления (внутримолекулярная и межмолекулярная(получаются простые эфиры) дегидратации),
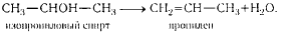
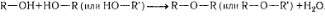
реакции окисления,
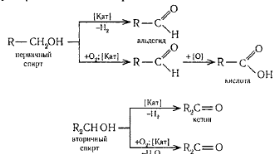
реакции поликонденсации (с кислотами).
Применение. Метиловый спирт - в производстве формальдегида, полупродукт в производстве муравьиной кислоты, метилацетата, метиламинов и многих красителей, фармацевтических препаратов, душистых веществ, в лакокрасочной промышленности, растворитель. Этиловый спирт - в производстве дивинила, этилового эфира, этилена высокой чистоты, антисептическое средство, растворитель.
 2015-04-17
2015-04-17 2768
2768
