Существует два способа уравнивания ОВР 1. метод электронного баланса; 2. метод электронно-ионного баланса (метод полуреакций). Метод электронного баланса Уравнивание ОВР основано на том, что число отданных и принятых ē должно быть одинаковым. Порядок уравнивания ОВР: 1.Находим элементы которые меняют СО; 2.Составляем схему передачи ē; 3.Уравниваем число отданных и принятых ē; 4.Выставляем коэффициент перед окислителем и восстановителем в молекулярном уравнении; 5.Уравниваем элементы которые не меняли СО. Например: 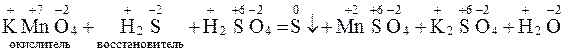 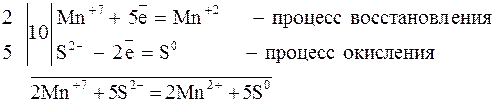 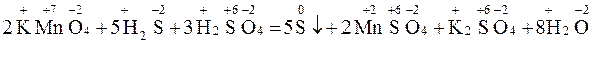 |
Метод электронно-ионного баланса (метод полуреакций) При составлении уравнений реакций по методу полуреакций (электронно-ионного баланса) необходимо следовать следующим правилам: 1.Соблюдать равенство суммарного числа электронов, отданных восстановителем и принятых окислителем. Электронный баланс сохраняет электронейтральность системы. 2.Сохранить число атомов исходных веществ в продуктах реакций независимо от изменения состава исходного соединения. Этот баланс основан на законе сохранения массы веществ при их химических превращениях. 3.Условно расчленить суммарный химический процесс на частные реакции – окислительную и восстановительную, в которых наряду с молекулами (ионами) участниками превращения являются электроны. Число электронов, отданных одной частицей восстановителя, является коэффициентом при молекуле (ионе) окислителя в суммарном уравнении. Аналогично число электронов, принятых окислителем, является коэффициентом при восстанавливающей частице. 4.Окислительная система – система, имеющая наибольшее значение стандартного электродного потенциала Аокисл.ф.I + nē ↔ Bвосст.ф.I Восстановительная система – это система, имеющая меньшее значение стандартного электродного потенциала Ввосст.ф.II – nē ↔ Аокисл.ф.II Суммарное уравнение реакции: Аокисл.ф.I + Ввосст.ф.II ↔ Аокисл.ф.II + Bвосст.ф.I 5.Реакции в водных растворах целесообразно отображать ионно-молекулярными уравнениями, так как обмен электронами осуществляется преимущественно при участии ионов веществ. Малорастворимые, твердые и газообразные вещества и слабо диссоциирующие вещества записываются только в молекулярной форме. Если реакция идет в кислой среде, то продуктами ее являются соли всех металлов данной кислоты и вода. 6.При составлении уравнения реакции с кислородсодержащими анионами (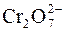 , , 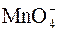 , , 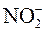 , , 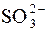 , , 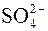 и т.д.) следует иметь в виду, что в водных растворах связывание избыточного кислорода и присоединение кислорода восстановителем происходит по-разному в кислой, нейтральной и щелочной средах. В кислых растворах избыток кислорода связывается ионами водорода с образованием молекул воды, а в нейтральных и щелочных – молекулами воды с образованием гидроксид-ионов, например: и т.д.) следует иметь в виду, что в водных растворах связывание избыточного кислорода и присоединение кислорода восстановителем происходит по-разному в кислой, нейтральной и щелочной средах. В кислых растворах избыток кислорода связывается ионами водорода с образованием молекул воды, а в нейтральных и щелочных – молекулами воды с образованием гидроксид-ионов, например: 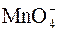 + 8H+ + 5ē ↔ Mn2+ + 4H2O – кислая среда; + 8H+ + 5ē ↔ Mn2+ + 4H2O – кислая среда;  + 6H2O + 8ē ↔ NH3 + 9OH– – нейтральная и щелочная среда. Присоединение кислорода восстановителем осуществляется в кислой и нейтральной средах за счет молекул воды с образованием ионов водорода, а в щелочной среде – за счет гидроксид-ионов с образованием молекул воды, например: I2 + 6H2O – 10ē ↔ 2 + 6H2O + 8ē ↔ NH3 + 9OH– – нейтральная и щелочная среда. Присоединение кислорода восстановителем осуществляется в кислой и нейтральной средах за счет молекул воды с образованием ионов водорода, а в щелочной среде – за счет гидроксид-ионов с образованием молекул воды, например: I2 + 6H2O – 10ē ↔ 2 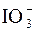 + 12H+ – кислая и нейтральная среда; + 12H+ – кислая и нейтральная среда; 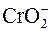 + 4OH– – 3ē ↔ + 4OH– – 3ē ↔ 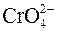 + 2H2O – щелочная среда. + 2H2O – щелочная среда. |
Например: а) K2Cr2O7 + H3PO3 + H2SO4 → Cr2(SO4)3 + H3PO4 + K2SO4 + H2O,
3 H3PO3 – 2ē + H2O = H3PO4 + 2H+ – процесс окисления Cr2O72– + 14H+ + 3H3PO3 + 3H2O = 3H3PO4+ 6H+ +2Cr3+ + 7H2O, после сокращения H2O и H+, имеем: Cr2O72– + 8H+ + 3H3PO3 = 3H3PO4 + 2Cr3+ + 4H2O, тогда молекулярное уравнение имеет вид: K2Cr2O7+3H3PO3+4H2SO4 = Cr2(SO4)3+3H3PO4+K2SO4+4H2O. K2Cr2O7 – окислитель; H3PO3 – восстановитель
3 SO32– – 2ē + 2ОН- = SO42–+ H2O – процесс окисления 2 MnO4– + 3ē + 2H2O = MnO2 + 4OH– – процесс восстановления 3SO32– + 6ОН– + 2MnO4– + после сокращения H2O и OH–, имеем: 3SO32– + 2MnO4– + H2O = 3SO42– + 2MnO2 + 2OH–, тогда молекулярное уравнение имеет вид: 3Na2SO3 +2 KMnO4 + H2O = 3 Na2SO4 + 2MnO2 + 2KOH. Na2SO3 – восстановитель; KMnO4 – окислитель. При уравнивании реакций методом электронно-ионного баланса (методом полуреакций) записываем две полуреакции – окисления и восстановления, в которых сильные электролиты пишем в виде ионов, а слабые – в виде молекул. Затем каждую полуреакцию уравниваем. Уравнивание полуреакций зависит от среды раствора. Если среда кислая, то для уравнивания используем ионы водорода Н+ и Н2О (добавляем где недостаток кислорода), а если щелочная – то гидроксо-группы ОН– и Н2О (добавляем где избыток кислорода). После этого уравниваем число отданных и принятых электронов, выставляем коэффициенты перед полуреакциями окислителя и восстановителя и записываем суммарное ионно-молекулярное уравнение с учетом выставленных коэффициентов. В полученном уравнении приводим подобные члены и переносим коэффициенты в молекулярное уравнение. |
 2015-04-01
2015-04-01 3897
3897

 1 Cr2O72– + 6ē + 14H+ = 2Cr3+ + 7H2O –
1 Cr2O72– + 6ē + 14H+ = 2Cr3+ + 7H2O –  б) Na2SO3 + KMnO4 + H2O → Na2SO4 + MnO2 + KOH,
б) Na2SO3 + KMnO4 + H2O → Na2SO4 + MnO2 + KOH,






