1. Соль образована ионами сильного основания и сильной кислоты (например, NaCl, KNO3 и др.).
NaCl + H2O  гидролиз не идет (NaOH - сильное основание, HCl - сильная кислота).
гидролиз не идет (NaOH - сильное основание, HCl - сильная кислота).
2. Соль образована ионами сильного основания и слабой кислоты (например, Na2CO3, KSCN и др.).
Na2CO3 + Н2О  гидролиз по аниону (NaOH - сильное основание, H2CO3 - cлабая кислота).
гидролиз по аниону (NaOH - сильное основание, H2CO3 - cлабая кислота).
CO32  + HOH
+ HOH 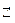 HCO3
HCO3  + OH
+ OH  (среда щелочная, рН>7).
(среда щелочная, рН>7).
Na2CO3+ HOH 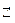 NaHCO3 + NaOH (1 ступень гидролиза).
NaHCO3 + NaOH (1 ступень гидролиза).
Добавление к раствору сильных щелочей (NaOH), содержащих одноименные ионы (OH  ), вызывает ослабление гидролиза (смещение равновесия влево по принципу Ле Шателье). Добавление к раствору кислот усиливает гидролиз за счет реакции Н++OH
), вызывает ослабление гидролиза (смещение равновесия влево по принципу Ле Шателье). Добавление к раствору кислот усиливает гидролиз за счет реакции Н++OH 
 Н2О, в результате которой концентрация ионов OH
Н2О, в результате которой концентрация ионов OH  в растворе уменьшается, и равновесие гидролиза смещается вправо. Гидролиз усиливается и начинает идти по второй ступени:
в растворе уменьшается, и равновесие гидролиза смещается вправо. Гидролиз усиливается и начинает идти по второй ступени:
НCO3  + HOH
+ HOH 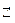 H2CO3 + OH
H2CO3 + OH 
NaНCO3 + HOH 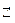 H2CO3 + NaOH (2 ступень гидролиза).
H2CO3 + NaOH (2 ступень гидролиза).
3. Соль образована ионами слабого основания и сильной кислоты (например, AlCl3, FeSO4 и др.).
AlCl3 + H2O  гидролиз по катиону (Al(OH)3 - слабое основание, НCl - cильная кислота).
гидролиз по катиону (Al(OH)3 - слабое основание, НCl - cильная кислота).
Al3+ + HOH 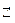 AlOH2+ + H+ (среда кислая, рН<7)
AlOH2+ + H+ (среда кислая, рН<7)
AlCl3 + HOH 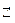 AlOHCl2 + HCl (1 ступень гидролиза).
AlOHCl2 + HCl (1 ступень гидролиза).
4. Соль образована ионами слабого основания и слабой кислоты:
а) соль растворима в воде (например, (NH4)2CO3, NH4NO2 и др.).
(NH4)2CO3 + H2O  гидролиз идет сразу по катиону и аниону:
гидролиз идет сразу по катиону и аниону:
2NH4+ + CO32  + HOH
+ HOH 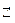 NH4OH + HCO3
NH4OH + HCO3  + NH4+ (рН
+ NH4+ (рН 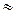 7)
7)
(NH4)2CO3 + HOH 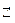 NH4OH + NH4HCO3
NH4OH + NH4HCO3
б) соль нерастворима в воде (например, FeS, ZnSiO3 и др.).
FeS + H2O  нерастворимые соли гидролизу не подвергаются;
нерастворимые соли гидролизу не подвергаются;
в) соль разлагается водой (в таблице растворимости стоит прочерк, например, Fe2S3, Al2(CO3)3 и др.). Гидролиз таких солей идет необратимо и до конца: Fe2S3+6H2O  2Fe(OH)3
2Fe(OH)3 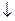 +3H2S
+3H2S 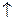
Цель работы. C помощью универсальной индикаторной бумаги определить реакцию среды водных растворов солей, изучить влияние температуры и концентрации на гидролиз, взаимное усиление гидролиза растворов различных солей.
Порядок работы.
Опыт 1. Определение рН в кислых, щелочных и
 2015-04-30
2015-04-30 5973
5973
