Оксокислоты – гетерофункциональные соединения, содержащие карбоксильную и карбонильную (альдегидную или кетонную) группы. В зависимости от взаимного расположения этих групп различают a -, b -, g - и т.д. оксокарбоновые кислоты.
Наиболее известными представителями этих классов соединений являются глицериновый альдегид и дигидроксиацетон, играющие в виде фосфатов большую роль в биохимических процессах.
Важную роль в биохимических процессах играют кетонокислоты - пировиноградная, ацетоуксусная и щавелевоуксусная

Гидроксикислоты дают реакции, характерные для карбоновых кислот и спиртов, при этом могут затрагиваться как одна, так и обе функции. Наиболее характерные реакции приведены на схеме.
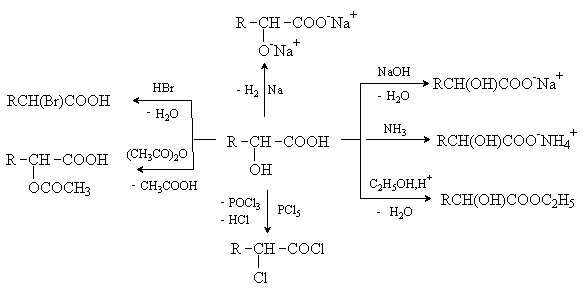
Кроме того, гидроксикислоты имеют ряд специфических свойств, обусловленных присутствием обеих групп и их взаимным расположением.
Отношение гидроксикислот к нагреванию.
Превращения гидроксикислот при нагревании определяются возможностью образования термодинамически стабильных 5-ти- 6-тичленных циклов
a -Гидроксикислоты вступают в реакцию межмолекулярного самоацилирования. При этом образуются циклические сложные эфиры – лактиды.
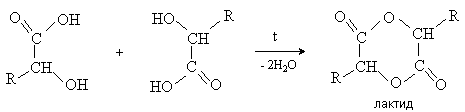
b -Гидроксикислоты при нагревании переходят a,b -непредельные кислоты.
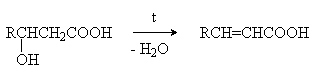
g - иd -Гидроксиокислоты претерпевают внутримолекулярное ацилирование с образованием циклических сложных эфиров – лактонов.
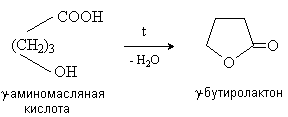
Специфические реакции a -гидроксикислот.
a -Гидроксикислоты образуют хелатные комплексы с ионами переходных металлов (Cu2+, Fe3+ и др.), которые содержат металл в составе устойчивого 5-тичленного цикла.
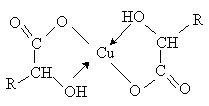
В присутствии минеральных кислот a -гидроксикислоты разлагаются с образованием муравьиной кислоты и соответствующего альдегида.
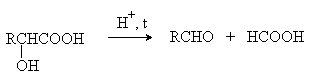
1.3. Биологически важные гидроксикислоты.
Гликолиевая кислота HOCH2COOH содержится во многих растениях, например, свекле и винограде.
Молочная кислота (соли лактаты) CH3CH(OH)COOH.
Широко распространена в природе, является продуктом молочнокислого брожения углеводов. Содержит асимметрический атом углерода и существует в виде двух энантиомеров. В природе встречаются оба энантиомера молочной кислоты. При молочнокислом брожении образуется рацемическая D,L-молочная кислота. D-молочная (мясо-молочная) кислота образуется при восстановлении пировиногралной кислоты под действием кофермента НАД Н и накапливается в мышцах при интенсивной работе.
| CH3COCOOH + НАД. Н + Н+ | ® | СH3CH(OH)COOH + НАД+ |
| Пировиноградная кислота | D-Молочная кислота |
Яблочная кислота (соли малаты) HOOCCH(OH)CH2COOH
Содержится в незрелых яблоках, рябине, фруктовых соках. Является ключевым соединением в цикле трикарбоновых кислот. В организме образуется путем гидратации фумаровой кислоты и далее окисляется коферментом НАД+ до щавелевоуксусной кислоты.
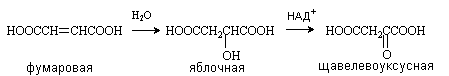
Лимонная кислота (соли цитраты)
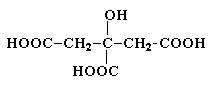
Содержится в плодах цитрусовых, винограде, крыжовнике. Является ключевым соединением в цикле трикарбоновых кислот. Образуется из щавелевоуксусной кислоты путем конденсации ее с ацетилкоферментом А и далее в результате последовательных стадий дегидратации и гидратации превращается в изолимонную кислоту.
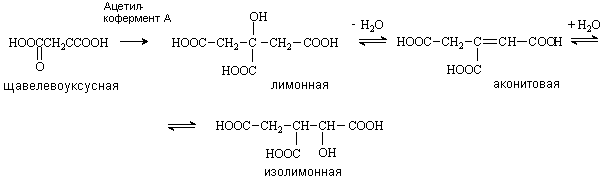
Винная кислота (соли тартраты) HOOCCH(OH)CH(OH)COOH.
Содержит два хиральных центра и имеет 3 стереоизомера: D-винную кислоту, L-винную кислоту и оптически неактивную мезовинную кислоту (см. лек. №4). D-винная кислота содержится во многих растения, например, в винограде и рябине. При нагревании D-винной кислоты образуется рацемическая D,L-винная (виноградная) кислота. Мезовинная кислота образуется при кипячении других стереоизомеров в присутствии щелочи и при окислении малеиновой кислоты (см. выше).
 2015-04-30
2015-04-30 3999
3999








