Процессы диссоциации важнейших для металлургии соединений – оксидов, нитридов, карбонатов – являются весьма важными, поскольку являются прямым способом получения металлов. Данные процессы весьма однотипны, и в зависимости от температуры их можно представить уравнениями вида:
АВтв = Атв + Вгаз;
АВтв = Аж + Вгаз;
АВж = Атв + Вгаз;
АВж = Аж + Вгаз.
Величина равновесного парциального давления газообразного продукта этих реакций называется упругостью диссоциации соединения АВ и характеризует прочность данного соединения. Реакции диссоциации являются эндотермическими, т.е. с повышением температуры равновесие смещается в сторону продуктов реакции. Уменьшение давления при сохранении состава газовой фазы оказывает аналогичное действие.
Согласно правилу фаз Гиббса, число степеней свободы для реакций диссоциации определяется как
С = К + 2 - Ф = 2 + 2 - 3 = 1,
т.е. для количественной характеристики достаточно лишь одного независимого параметра – температуры, от которой зависит константа равновесия процесса:
Кр = РВ = ¦ (Т).
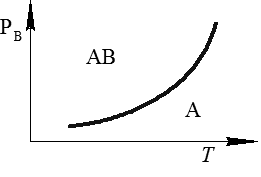
Рис. 3.1. Зависимость упругости диссоциации соединения АВ от температуры
На рис. 3.1 представлена зависимость РВ от температуры для указанных реакций.
 2015-05-05
2015-05-05 1338
1338








