В черной металлургии наибольший практический интерес представляет анализ реакции диссоциации карбонатов кальция СаСО3, магния MgCO3, марганца MnCO3, железа FeCO3 (сидерит) и доломита CaMg(CO3)2. Процессы диссоциации этих соединений однотипны и протекают по уравнению:
MeCO3 = MeO + CO2,
Kp = 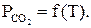
Величина 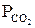 является упругостью диссоциации карбоната и характеризует меру химической прочности соединения.
является упругостью диссоциации карбоната и характеризует меру химической прочности соединения.
Наибольший интерес представляет реакция диссоциации карбоната кальция, который входит в состав шихтовых материалов доменного и сталеплавильного производства, а также используется для получения СаО через обжиг известняка.
Реакция диссоциации СаСО3 описывается уравнением вида
СаCO3 = СаOтв + CO2, 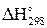 = 177 400 Дж; (3.1)
= 177 400 Дж; (3.1)
DG°Т = 178 070 - 150 Т; Kp(3.1) = 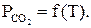
Зависимость упругости диссоциации карбоната 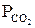 от температуры представлена на рис. 3.2.
от температуры представлена на рис. 3.2.
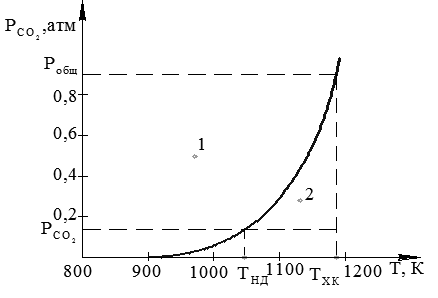
Рис. 3.2. Упругость диссоциации СаСО3
Анализ данной графической зависимости с использованием изотермы химической реакции показывает, что диссоциация карбоната возможна, когда фактическое значение 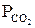 меньше равновесного и при этом DG°Т < 0. Температура, при которой возможен этот процесс, является температурой начала диссоциации ТНД.
меньше равновесного и при этом DG°Т < 0. Температура, при которой возможен этот процесс, является температурой начала диссоциации ТНД.
Любая фигуративная точка 1 выше равновесной линии на рис. 3.2 отвечает устойчивому существованию карбоната СаСО3. Любая фигуративная точка 2 ниже линии отвечает устойчивому существованию оксида СаО.
Процесс диссоциации карбоната протекает с высокой скоростью при температурах выше температуры химического кипения ТХК, при которой упругость диссоциации становится равной общему внешнему давлению газовой фазы.
 2015-05-05
2015-05-05 3814
3814
