Федеральное агентство по образованию
Южно-Уральский государственный университет
Филиал в г. Златоусте
Кафедра «Общая металлургия»
669.02/.09(07)
Д463
А.Н. Дильдин
ТЕОРИЯ МЕТАЛЛУРГИЧЕСКИХ ПРОЦЕССОВ
Учебное пособие
Челябинск
Издательство ЮУрГУ
ВВЕДЕНИЕ
Металлургические процессы – это совокупность физических явлений и физико-химических превращений (движение газов, жидких и твердых материалов, тепло- и массообмен, фазовые переходы, окисление и восстановление материалов и т.п.), происходящих в металлургических агрегатах (доменная печь, агломерационная машина, сталеплавильная и нагревательная печи, конвертер) при высоких температурах. Предметом изучения курса «Теория металлургических процессов» являются реакции, протекающие в указанных металлургических агрегатах.
Курс ТМП занимает особое положение среди всех металлургических дисциплин, по сути, он является прикладной физической химией применительно к анализу явлений, происходящих при производстве чугуна, стали и ферросплавов.
Теоретические основы металлургических процессов рассматриваются в определенной последовательности: вначале на основе законов термодинамики анализируются условия равновесия химических процессов, затем – кинетика и особенности механизма процессов. Эти вопросы и являются основными задачами, решаемыми при изучении курса ТМП.
СОСТАВ И СВОЙСТВА ВЫСОКОТЕМПЕРАТУРНОЙ ГАЗОВОЙ АТМОСФЕРЫ
Термодинамика газовых атмосфер
Пирометаллургические процессы производства металлургических расплавов (чугун, сталь, сплав) протекают с участием газовых атмосфер, которые могут быть нейтральными, окислительными и восстановительными.
Состав, давление и температура газовой фазы зависят от характера ее взаимодействия с другими фазами, образующимися при получении металлов и сплавов. При этом как промежуточный, так и полный состав газовой фазы весьма однотипен:
продукты полного взаимодействия элементов с кислородом – CO2, H2O(пар), SO3;
продукты неполного взаимодействия с кислородом, диссоциации оксидов и дегазации металлов – CO, SO2, H2,, O2, N2, CH4; инертные газы – Ar, Kr.
Равновесный состав газовой фазы можно рассчитать на основе термодинамического анализа химических реакций, важнейшими из которых являются реакции взаимодействия с кислородом водорода, окиси углерода, метана и сернистого ангидрида.
Данные обратимые реакции описываются следующими химическими уравнениями (на 1 моль О2):
| 2H2 + O2 = 2H2O(пар), | 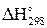 = - 484 660 Дж; = - 484 660 Дж;
| (1.1) |
| 2СО + O2 = 2СО2, | 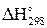 = - 566 350 Дж; = - 566 350 Дж;
| (1.2) |
| 2СH4 + O2 = 2СО + 4H2O, | 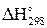 = - 71 360 Дж; = - 71 360 Дж;
| (1.3) |
| 1/2СH4 + O2 = 1/2СО2 + Н2О, | 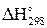 = - 401 740 Дж; = - 401 740 Дж;
| (1.4) |
| 2SO2 + O2 = 2SO3, | 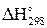 = - 196 850 Дж. = - 196 850 Дж.
| (1.5) |
Термодинамический анализ данных обратимых реакций позволяет установить равновесные содержания и парциальные давления молекулярного кислорода, а также охарактеризовать окислительно-восстановительные свойства газовой фазы в указанных реакциях.
Рассчитать тепловые эффекты DНТ экзотермических реакций (1.1)–(1.5) при высоких температурах можно по уравнению Кирхгофа с использованием табличных данных для определения теплоемкостей процессов [1].
Однако более важной термодинамической характеристикой, которая определяет направление протекания химических реакций, является изменение энергии Гиббса DGТ, стандартное изменение которой DG°Т, в зависимости от температуры для реакций (1.1)–(1.5) имеет вид, Дж:
DG°(1.1) = - 492 200 + 108 Т;
DG°(1.2) = - 565 400 + 175 Т;
DG°(1.3) = - 71 000 + 370 Т;
DG°(1.4) = - 398 230 + 2 Т;
DG°(1.5) = - 196 840 + 196 Т.
На рис. 1.1 представлены графики этих зависимостей.
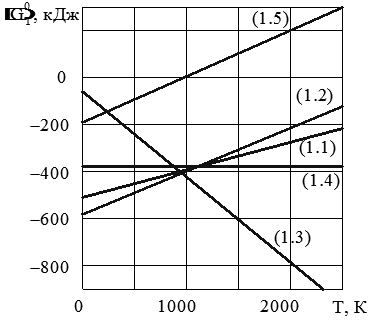
Рис. 1.1. Стандартная энергия Гиббса для реакций горения
Указанные зависимости справедливы при температуре до 2500 К и общем давлении в системе Р=1 атм., т.е. до процессов диссоциации H2О, O2, Н2 на атомы, их ионизации и образования плазмы.
Из анализа приведенных зависимостей и графиков вида DG°Т = f(Т) на рис. 1.1 следует, что с повышением давления равновесие реакций (1.1), (1.2) и (1.5) смещается в прямом направлении, а с повышением температуры полнота протекания этих реакций уменьшается. Изменение давления не влияет на равновесие реакции (1.4), а прямой ход реакции (1.3) с увеличением давления замедляется. С повышением температуры реакции (1.3) и (1.4) характеризуются большей полнотой протекания.
Равновесный состав образовавшейся атмосферы и парциальные давления ее составляющих компонентов позволят определить и рассчитать окислительно-восстановительные свойства (ОВС) газовой фазы, воздействующей на способные к окислению или восстановлению материалы гетерогенной системы.
Простейшей количественной характеристикой ОВС какой-либо газовой смеси является равновесное парциальное давление кислорода 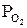 . Однако более точной оценкой ОВС газовой атмосферы является ее кислородный потенциал pО, представляющий собой величину химического потенциала молекулярного кислорода при отсчете его от стандартного состояния, при котором
. Однако более точной оценкой ОВС газовой атмосферы является ее кислородный потенциал pО, представляющий собой величину химического потенциала молекулярного кислорода при отсчете его от стандартного состояния, при котором 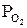 = 1 атм.:
= 1 атм.:
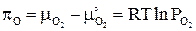 . (1.6)
. (1.6)
Величина pО зависит от температуры и от состава газовой фазы, который выражается через отношение парциальных давлений реагентов, влияющих на 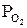 .
.
В металлургических агрегатах газовые атмосферы состоят из множества компонентов, которые постоянно участвуют в физико-химических превращениях. Термодинамический анализ таких систем основывается на утверждении, что сложное химическое равновесие достигается в результате одновременного установления в системе всех возможных частных равновесий.
Так, при одновременном протекании в газовой фазе реакций (1.1)–(1.5) при T=const давления указанных компонентов примут значения, соответствующие константам равновесия КР(1.1)–КР(1.5), а кислородный потенциал газовой смеси
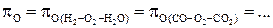
может быть рассчитан по данным любого из этих равновесий, например, по уравнению
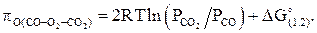 (1.7)
(1.7)
В рассматриваемой восьмикомпонентной газовой смеси помимо реакций (1.1)–(1.5) возможны и другие химические взаимодействия между реагентами. Наибольший интерес представляет так называемая реакция водяного газа (водяным газом называют смесь четырех газов Н2 – Н2О – СО – СО2):
Н2 + СО2 = Н2О + СО, DG°(1.5) = 36 600 - 33,5T Дж. (1.8)
Анализ этой реакции исключительно важен в металлургии для оценки равновесий в газовых атмосферах при использовании природного газа или увлажненного дутья в доменной печи, других металлургических агрегатах.
Для определения равновесного состава системы реакции (1.8) нужно задаваться не только значением константы равновесия
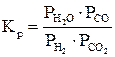 (1.9)
(1.9)
и общим давлением
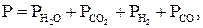 (1.10)
(1.10)
но и еще двумя какими-либо условиями, что следует из анализа числа степеней свободы:
С = p + 2 - Ф = 3 + 2 - 1 = 4.
На практике чаще всего задают исходный состав системы или парциальные давления паров в исходной смеси. В нашем случае кроме Р и Т в качестве двух переменных можно выбрать не изменяющиеся числа молей углерода и водорода или не изменяющиеся суммы парциальных давлений водорода и углеродсодержащих газов:
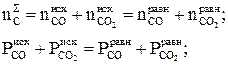 (1.11)
(1.11)
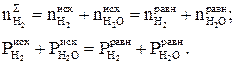 (1.12)
(1.12)
Совместное решение уравнений (1.9)–(1.12) позволяет найти равновесный состав газовой смеси. Результаты расчетов можно представить графически, при этом исходными данными являются соотношения:
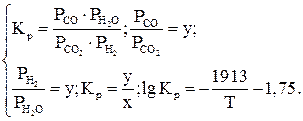 (1.13)
(1.13)
Из графика (рис. 1.2) при заданной температуре и 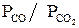 можно определить равновесное с ним отношение
можно определить равновесное с ним отношение 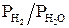 и наоборот. После вычисления равновесного значения %СО / %СО2 (или %Н2 / %Н2О) можно определить кислородный потенциал системы СО – СО2 – Н2 – Н2О и нанести на рис. 1.2 линии постоянных значений pО.
и наоборот. После вычисления равновесного значения %СО / %СО2 (или %Н2 / %Н2О) можно определить кислородный потенциал системы СО – СО2 – Н2 – Н2О и нанести на рис. 1.2 линии постоянных значений pО.
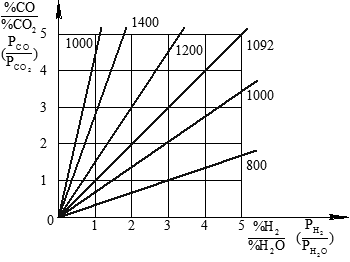
Рис. 1.2. Соотношение между %СО / %СО2 и %Н2 / %Н2О.
 2015-05-05
2015-05-05 1603
1603