Уравнением состояния или термическим уравнением состояния называется функция f(P,V,T)=0, связывающая все макропараметры системы (ИГ). Получают его, следуя Б.П.Э. Клайперону (1799–1864) и Д.И. Менделееву (1834–1907 гг.).
Изменение состояния ИГ в результате двух изопроцессов (сначала изотермического, а затем изохорного), изображено на рис. 9.2.
Соответственно получают: P 1 V 1= P '1 V 2 и 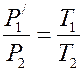 . Исключая из уравнений величину P '1, получают уравнение Клапейрона:
. Исключая из уравнений величину P '1, получают уравнение Клапейрона:
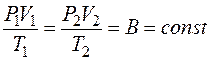 . (9.6)
. (9.6)
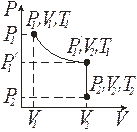
Рис. 9.2
Так как все состояния ИГ были выбраны произвольно, то уравнение (9.6) выполняется в любом ТД процессе для данной массы m ИГ (значение постоянной В зависит от природы газа).
Менделеев объединил уравнение Клапейрона с законом Авогадро. Так как при данных давлении и температуре газы занимают одинаковый объем, для одного моля газа можно записать:
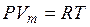 , (9.7)
, (9.7)
где R – универсальная газовая постоянная, не зависящая от природы ИГ R = k × NA =8,31 Дж/(моль×К).
Чтобы перейти к произвольной массе газа, заметим, что объем, который занимают v молей газа в v раз больше молярного объема Vm, т.е. V=nVm (по пропорции 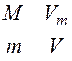 (М – масса одного моля (молярная масса) газа) с учетом n=m/M получают то же V=nVm). Тогда
(М – масса одного моля (молярная масса) газа) с учетом n=m/M получают то же V=nVm). Тогда
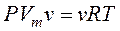 (9.8)
(9.8)
или
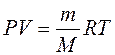 . (9.8')
. (9.8')
Иногда уравнение (9.8) записывают в виде
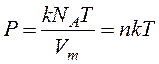 , (9.9)
, (9.9)
где n – концентрация частиц вещества (атомов, молекул).
В рамках модели ИГ получим основное уравнение МКТ, связывающее давление газа с механическими характеристиками молекул – скоростью и энергией.
Молекулы газа движутся с различными скоростями, поэтому для упрощения используют квадратичное усреднение 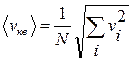 :
:
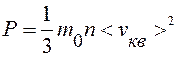 . (9.11)
. (9.11)
Уравнение (9.11) – основное уравнение МКТ. Учитывая, что n=N/V, уравнение (9.11) можно записать в виде:
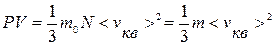 или
или 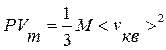 . (9.12)
. (9.12)
С учетом уравнения (9.7) получают
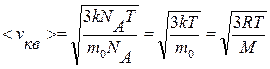 . (9.13)
. (9.13)
Для воздуха (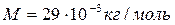 )
) 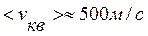 .
.
Средняя кинетическая энергия поступательного движения одной молекулы:
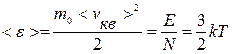 . (9.14)
. (9.14)
С учетом уравнения (9.14) основное уравнение МКТ можно записать в следующем виде:
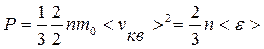 . (9.15)
. (9.15)
При Т =0 К поступательное движение молекул прекращается и газ не оказывает давления на сосуд.
 2015-05-05
2015-05-05 1300
1300
