Задание 1. Определение 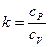 воздуха.
воздуха.
1.1 Закройте кран 5, откройте кран 6и насосом 3 закачайте в баллон воздух до давления 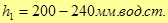 и закройте кран 6
и закройте кран 6
2.2 Наблюдайте за показанием манометра 4: давление будет уменьшаться и через некоторое время (обычно 3-5 минут) разность уровней в коленах манометра установится неизменной. Это означает, что температура газа в баллоне стала равна комнатной. Этому состоянию соответствует точка 1 на рис.6. Запишите значение 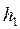 в таблицу 4
в таблицу 4
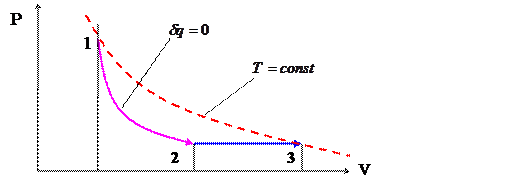
1.2. Откройте быстро кран 5, повернув его рукоятку на 900;газ начнет расширяться по линии 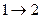 ); как только разность уровней жидкости в манометре станет равной нулю, закройте кран. Состоянию газа при закрытия крана соответствует точка 2 на рис.4. Далее процесс пойдет изохорно по линии
); как только разность уровней жидкости в манометре станет равной нулю, закройте кран. Состоянию газа при закрытия крана соответствует точка 2 на рис.4. Далее процесс пойдет изохорно по линии 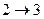 , температура и давление будут увеличиваться. После установления неизменного давления запишите значение
, температура и давление будут увеличиваться. После установления неизменного давления запишите значение 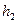 .Повторите опыты 5-6 раз, данные – в таблицу 4.
.Повторите опыты 5-6 раз, данные – в таблицу 4.
1.3. Проведите несколько опытов с выпуском воздуха из горлышка баллона::после установления режима в точке 1 быстро вынимается пробка 2 и практически сразу же вставляется обратно на место – промежутка времени между этими действиями вполне хватает для полного выпуска воздуха Данные запишите в отдельную таблицу или в продолжение таблицы 4.
1.4. Вычислите для всех контрольных опытов значения 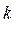 и определите среднее его значение
и определите среднее его значение
Таблица 4
| №№ опыта | 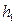
| 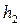
| 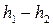
| 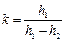
|
Среднее значение 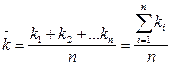
|
1.5 Определите параметры состояния воздуха в точках 1, 2.и 3: температуру, давление, удельный объем, внутреннюю энергию, энтальпию. Внутреннюю энергию 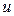 и энтальпию
и энтальпию 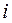 считать равными нулю при нормальных условиях (Н.У):
считать равными нулю при нормальных условиях (Н.У):
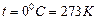
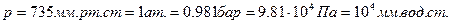
Тогда их значения определяются по формулам:
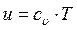 , и
, и 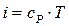 (49)
(49)
Теплоемкость воздуха брать равной 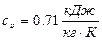 ,
, 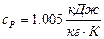
Точка 1. Температура 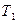 и давление
и давление 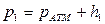 непосредственно измеряются, удельный объем вычисляется из уравнения состояния идеального газа для 1 кг газа
непосредственно измеряются, удельный объем вычисляется из уравнения состояния идеального газа для 1 кг газа
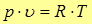 (50)
(50)
здесь 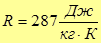 - газовая постоянная исследуемого газа (воздуха)
- газовая постоянная исследуемого газа (воздуха)
Внутренняя энергия и энтальпия определяются по формулам (64)
Точка 2. Для определения удельного объема газа используйте уравнение адиабаты для процесса 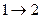 в виде:
в виде:
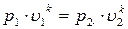
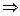
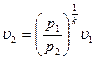 (51)
(51)
Зная давление и объем, определите температуру 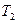 газа через уравнение Клапейрона-Менделеева и после этого - внутреннюю энергию
газа через уравнение Клапейрона-Менделеева и после этого - внутреннюю энергию 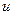 и энтальпию
и энтальпию 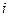
Точка 3. Температура 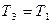 , давление
, давление 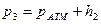 ; удельный объем определяете по уравнению (50), внутреннюю энергию и энтальпию - по формулам (49).
; удельный объем определяете по уравнению (50), внутреннюю энергию и энтальпию - по формулам (49).
Параметры точек внесите в таблицу 5
Таблица 5
| №№ точек | Температура | Давление | Удельный объем | Внутренняя энергия | Энтальпия. |
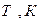
| 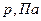
| 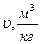
| 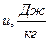
| 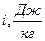
| |
Задание 2. Определение зависимости 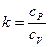 от длительности истечения воздуха.
от длительности истечения воздуха.
2.1 От угла поворота рукоятки крана 5 зависит его выходное сечение, которое влияет на время истечения (расширения) газа, что в свою очередь влияет на степень адиабатичности процесса. Для того чтобы убедится в этом, проведите 5-6 опытов при разных положениях рукоятки крана, измеряя время 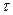 , в течение которого происходит выравнивание уровней жидкости в манометре после открытия крана. Время
, в течение которого происходит выравнивание уровней жидкости в манометре после открытия крана. Время 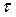 нельзя задать заранее, оно определяется в ходе опыте. Приведенные в таблице 6 значения
нельзя задать заранее, оно определяется в ходе опыте. Приведенные в таблице 6 значения 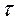 - ориентировочные
- ориентировочные
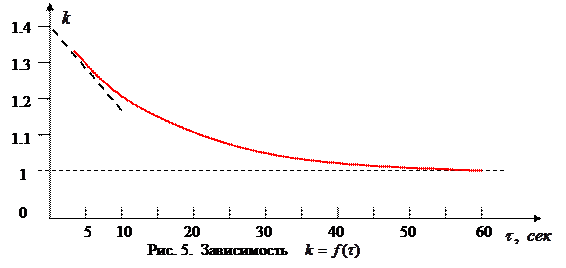
2.2 По полученным значениям 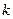 постройте график зависимости
постройте график зависимости 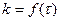 (его вид показан на рис. 5)
(его вид показан на рис. 5)
Таблица 6
| №№ опыта | Угол поворота крана | Время истечения
газа, 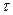 , сек , сек
| 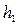 мм
мм
| 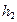 мм
мм
| 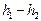 мм
мм
| 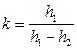
|
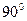
| 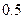
| |||||
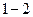
| ||||||
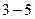
| ||||||
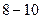
| ||||||
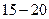
| ||||||
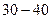
| ||||||
| ||||||
|
.
При увеличении времени истечения коэффициент 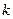 стремится к значению показателя политропы для изотермического процесса (
стремится к значению показателя политропы для изотермического процесса (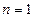 ) Экстраполируя график в направлении
) Экстраполируя график в направлении 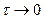 до пересечении с вертикальной осью
до пересечении с вертикальной осью 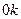 , находим значение показателя адиабаты при «мгновенном» расширении газа, которое и соответствует (теоретически) адиабатичности процесса
, находим значение показателя адиабаты при «мгновенном» расширении газа, которое и соответствует (теоретически) адиабатичности процесса
Контрольные вопросы, задачи
1. Что такое теплоемкость? Какие есть виды теплоемкости?
2. Теплоемкость идеального газа с точки зре6ия молеклярно-кинетической теории.
Теплоемкость смеси газов.
3. Удельная массовая теплоемкость 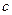 связана с объемной теплоемкостью
связана с объемной теплоемкостью 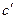 формулой
формулой
А) 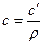 ; В)
; В) 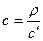 ; С)
; С) 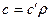 ; D)
; D) 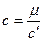 ; E)
; E) 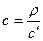
4. Первый закон термодинамики. Теплота. Внутренняя энергия. Энтальпия. Работа расширения газа. Работа проталкивания.
5. Как соотносятся величины внутренней энергии стакана воды на столе на кухне и на столе в
летящем на высот 10 км самолете?
6. Уравнение Майера; вывод этого уравнения Применимо ли уравнение Майера для капельных жидкостей (например, воды)?
7. Адиабатный процесс; у равнение адиабаты; теплоемкость адиабатного процес
8. Политропный процесс.Уравнение политропы. Теплоемкость политропного процесса.
9. Значения показателя политропы 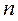 в разных процессах
в разных процессах
10. Есть ли обмен энергией между системой и средой в адиабатном процессе?
11. Получите выражение для определения доли теплоты, сообщенной газу в изобарном процессе, идущей на изменение внутренней энергии и доли, идущей на совершение работы.
12. Выражения для работы расширения газа в разных изопроцессах
13. Метод Клемана-Дезорма. Возможные причины погрешностей при определении показателя адиабаты в этом методе.
14. На рисунке изображены несколько процессов, протекающих с идеальным газом. Как ведет себя внутренняя энергия в ходе каждого процесса?
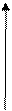



 1
1
Р 2
5 3 изотерма
4 адиабата
V
15. Сравните изменение температур в трех процессах (0-1, 0-2, 0-3) с идеальным газом, приведенных в Р -υ координатах
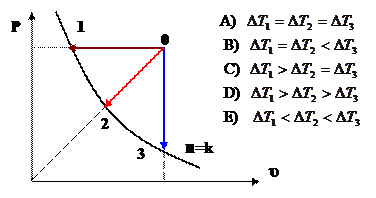
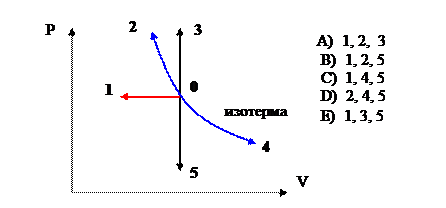
16. На рисунке в Р-V координатах приведены процессы с идеальным газом, начинающиеся в точке О. В каких процессах теплота отводится от газа?
 |
17. П олучите формулу, по которой можно определить отношение изменений энтальпии и внутренней энергии
18. Состояние идеального газа изменяется в соответствии с уравнением Р = kV, где 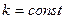 . Определите работу, совершаемую молем газа при повышении его температуры от Т 1 до Т2
. Определите работу, совершаемую молем газа при повышении его температуры от Т 1 до Т2
19. Сравните изменение энтальпий в трех процессах (0-1, 0-2, 0-3) с идеальным газом, приведенных на Р -υ диаграмме
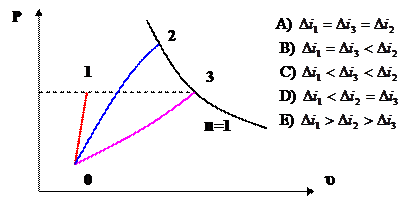
20. В Р-V диаграмме приведен процесс c показателем политропы 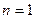 с идеальным газом. Что можно сказать о теплоте процесса 1-2?
с идеальным газом. Что можно сказать о теплоте процесса 1-2?
 |
А) теплота отводится; В) теплота подводится
С) теплота не подводится и не отводится; D) нельзя ответить однозначно
21. Нанесите) на кривой цикла с идеальным газом в 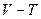 координатах:
координатах:
1) точку 1, в которой минимально давление газа
 2) точку 2, в которой максимально произведение давления газа на объем б)
2) точку 2, в которой максимально произведение давления газа на объем б)
22. Некоторое количество идеального газа совершает процесс 1-2-3 (один период
синусоиды) Как изменяются указанные в таблице величины?
 Р 3
Р 3

 |
V

| А | В | С | D | ||
| Работа | 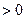
| 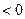
| 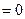
| Нельзя сказать определенно | |
| Теплота | Подводится к системе | Отводится от системы | 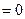
| Нельзя сказать определенно | |
| Внутренняя энергия | 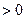
| 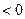
| 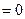
| Нельзя сказать определенно | |
| Температура | 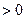
| 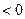
| 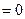
| Нельзя сказать определенно | |
| Энтальпия | 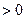
| 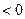
| 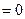
| Нельзя сказать определенно |
23. Как изменяется давление данной массы идеального газа на каждом участке в процессе, показанном на рисунке ниже?
 V, м3
V, м3
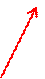


1 3
T, K

Процесс 1-2: А) не меняется В) увеличивается
С) уменьшается D) нельзя сказать определенно
Процесс 2-3: А) не меняется В) увеличивается
С) уменьшается D) нельзя сказать определенно
Процесс 3-1: А) не меняется В) увеличивается
С) уменьшается D) нельзя сказать определенно
24. Некоторое количество идеального газа совершает процесс 1-2-3 (один период
синусоиды) Как изменяются указанные в таблице величины?
 Р
Р

 3
3
V

| А | В | С | D | ||
| Работа в процессе | 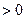
| 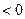
| 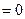
| Нельзя сказать определенно | |
| Теплота процесса | Подводится к системе | Отводится от системы | 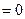
| Нельзя сказать определенно | |
| Внутренняя энергия | 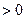
| 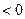
| 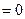
| Нельзя сказать определенно | |
| Температура в процессе | 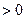
| 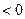
| 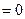
| Нельзя сказать определенно | |
| Энтальпия в процессе | 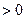
| 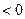
| 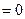
| Нельзя сказать определенно |
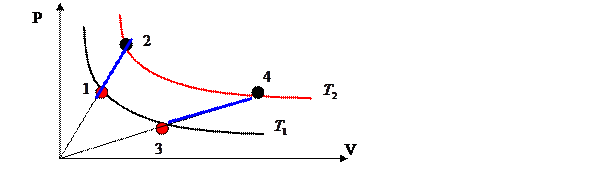
25. Между двумя изотермами идеального газа 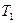 и
и 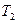 проводятся процессы 1-2 и 3-4, продолжения линий которых проходят через начало координат
проводятся процессы 1-2 и 3-4, продолжения линий которых проходят через начало координат
1) Как соотносятся работы 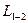 и
и 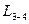 в этих процессах?
в этих процессах?
2) Как соотносятся теплоты 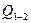 и
и 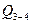 в этих процессах?
в этих процессах?
| Работа | 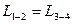
| 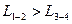
| 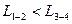
| Нельзя сказать определенно | 0.5 б | |
| Теплота | 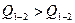
| 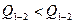
| 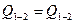
| Нельзя сказать определенно | 0.5 б |
3) Обоснование ответов
26 (204 Р) Работа, затраченная на адиабатное сжатие 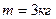 воздуха, составляет
воздуха, составляет 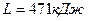 . Начальное состояние воздуха характеризуется параметрами
. Начальное состояние воздуха характеризуется параметрами 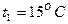 ;
; 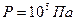 . Определить конечную температуру и изменение внутренней энергии Ответ
. Определить конечную температуру и изменение внутренней энергии Ответ 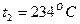 ;
; 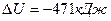 )
)
27. Воздух массой 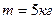 при температуре
при температуре 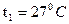 сжимается адиабатно до объема, cоставляющего 1/10 начального (
сжимается адиабатно до объема, cоставляющего 1/10 начального (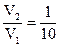 ), а затем расширяется изотермически до первоначального объема.
), а затем расширяется изотермически до первоначального объема.
1) Приведите эти процессы в 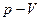 координатах.
координатах.
2) Определите работу, произведенную воздухом в результате обоих процессов
28.. Как изменяется давление данной массы идеального газа на каждом участке в цикле, показанном на рисунке ниже? (1 б)
 V, м3
V, м3

 2
2

 1 3
1 3
 T, K
T, K
Процесс 1-2: А) не меняется В) увеличивается
С) уменьшается D) нельзя сказать определенно
Процесс 2-3: А) не меняется В) увеличивается
С) уменьшается D) нельзя сказать определенно
Процесс 3-1: А) не меняется В) увеличивается
29. Совершается ли работа в изотермическом процессе?
A) Да
B) Нет
C) Нельзя сказать определенно
30. Может ли система совершать работу без подвода тепла извне?
A) Да
B) Нет
C) Нельзя сказать определенно
31. На рисунке в 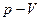 коодинатах приведен процесс
коодинатах приведен процесс 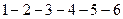 с идеальным газом.
с идеальным газом.
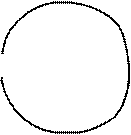
1) Какой величине геометрически численно равна работа в этом процессе?
2) Какой знак имеет работа?
Примечание: точки 1 и 5, а также 3 и 6 совпадают, но на рисунке они частично разделены для того, чтобы показать траекторию движения в процессе

 Р 2
Р 2
 |




 1 3
1 3
 5 6
5 6


7 8
 32. Определить количество тепла, необходимого для перевода четырех молей двух-
32. Определить количество тепла, необходимого для перевода четырех молей двух-
атомного газа из точки 1 в точку 2. В точке 1 температура газа Т1 = 500 К
33. Сравните изменения внутренней энергии  по абсолютной величине в трех приведенных на рисунке процессах 0-1, 0-2 и 0-3
по абсолютной величине в трех приведенных на рисунке процессах 0-1, 0-2 и 0-3

34. Воздух массой m = 1 кг при температуре t1 = -20 0С и давлении p1 = 0.1 МПа адиабатно сжимается до давления p2 = 0.8 МПа. Определить удельный объем воздуха и его температуру в конце сжатия и затраченную работу.
35. Укажите двухсторонней стрелкой область, где внутренняя энергия газа увеличивается в ходе любого процесса, начало которого лежит в точке 1. (Справа показан пример проведения стрелки)
36. На рисунке приведен цикл идеального газа в V-Т координатах. Постройте этот цикл в P-T- координатах. Масштаб-произвольный, но сохранить закономерности
 |
37 В двух одинаковых цилиндрах под поршнями находится одинаковое количество воздуха при одинаковых начальных условиях.. К цилиндрам подвели одинаковое количество теплоты.  В цилиндре
В цилиндре 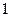 процесс протекает при
процесс протекает при 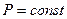 , в цилиндре
, в цилиндре 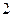 - при
- при 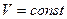 .
.
1) Как соотносятся изменения температур 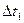 и
и 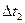 в цилиндрах?
в цилиндрах?
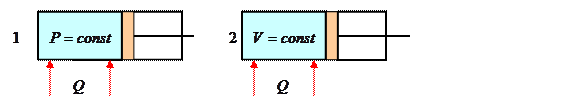
А) 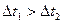 ; В)
; В) 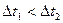 ; С)
; С) 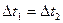 ; D) нельзя сказать определенно.
; D) нельзя сказать определенно.
2) Обоснование ответа
38. Некоторое количество идеального газа переходит из состояния 1 в состояние 2 (см. рисунок)

 Р 2
Р 2
 |
 |
V

1. Совершается ли работа газом в процессе 1-2?
A) Да
B) Нет
C) Нельзя сказать определенно
3 Получает или отдает газ теплоту в процессе 1-2?
A) Да
B) Нет
C) Нельзя сказать определенно
4. Как изменяется внутренняя энергия газа в процессе 1-2?
А) не меняется, В) увеличивается,
C) нельзя сказать определенно D) уменьшается
5. Как изменяется энтальпия а газа в процессе 1-2?
А) не меняется, В) увеличивается,
C) нельзя сказать определенно D) уменьшается
4. Как изменяется температура газа в процессе?
А) не меняется, В) увеличивается,
C) нельзя сказать определенно D) уменьшается
39. Воздух массой m = 1 кг при температуре t1 = 40 0С сжимается адиабатно до объема, cоставляющего 1/10 начального, а затем расширяется изотермически до первоначального объема. Определить работу, произведенную воздухом в результате обоих процессов.
40. Когда мы пытаемся сжать газ (например, перемещая в цилиндре поршень вправо), то встречаем этому сопротивление. Означает ли это, что молекулы газа в цилиндре при этом отталкиваются друг от друга (как например, одноименные электрические заряды)?
 |
41. Когда мы пытаемся увеличить объем газа в цилиндре (перемещая поршень влево), то вновь встречаем этому сопротивление. Означает ли это, что молекулы газа в цилиндре притягиваются (как разноименные электрические заряды)?
42. Некоторое количество двухатомного идеального газа расширяется: сначала адиабатно (по линии 1-2) а затем – изобарно (по линии 2-3). Конечная температура газа равна начальной (Т 1= Т3) При адиабатном расширении газ совершает работу, равную 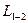 Чему равна работа
Чему равна работа 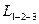 газа за весь процесс?
газа за весь процесс?
(ответ: 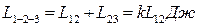 )
)
 2015-05-06
2015-05-06 1879
1879








