- декстрин
- гликоген
- крахмал
- целлюлоза
Белки - главные «труженики» клетки — это природные биополимеры, построенные из остатков 20 аминокислот. В состав макромолекул белков может входить от нескольких десятков до сотен тысяч и даже миллионов аминокислотных остатков, причем свойства белка существенно зависят именно от порядка, в котором располагаются эти остатки друг за другом. Поэтому, очевидно, что число возможных белков практически не ограничено.
Аминокислотами называют органические соединения, в которых карбоксильная (кислотная) группа СООН и аминогруппа NH2. присоединены к одному и тому же атому углерода.
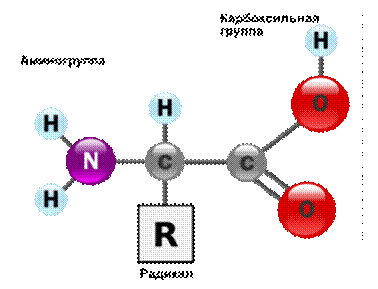
Рис.1 Структурная формула аминокислот
Строение такой молекулы описывается структурной формулой (рис.1), где R - радикал, разный для разных аминокислот. Таким образом, в состав аминокислот входят все четыре органогена С, О, Н, N, а в некоторые радикалы может входить сера S.
По способности человека синтезировать аминокислоты из их предшественников они делятся на две группы:
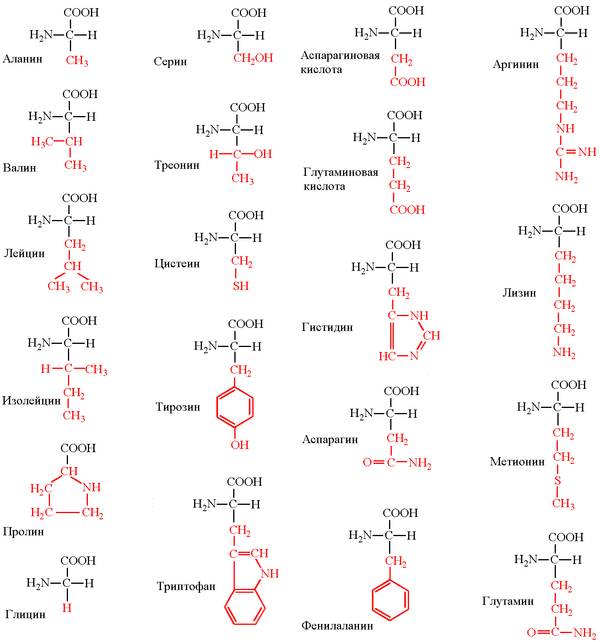
- Незаменимые: Триптофан, Фенилаланин, Лизин, Треонин, Метионин, Лейцин, Изолейцин, Валин, Аргинин, Гистидин;
- Заменимые: Тирозин, Цистеин, Глицин, Аланин, Серин, Глутаминовая кислота, Глутамин, Аспарагиновая кислота, Аспарагин, Пролин
Незаменимые аминокислоты должны поступать в организм человека с пищей, так как они не синтезируются человеком, хотя некоторые заменимые аминокислоты синтезируются в организме человека в недостаточных количествах и тоже должны поступать с пищей.
Химические формулы 20 стандартных аминокислот:
Структуру белковой молекулы, поддерживаемую ковалентными связями между аминокислотными остатками, называют первичной. Другими словами, первичная структура белка определяется простой последовательностью аминокислотных остатков. Эти остатки могут вполне определенным образом размещаться в пространстве, образуя вторичную структуру. Наиболее характерной вторичной структурой является α-спираль, когда аминокислотные цепочки как бы образуют резьбу винта.
Одним из самых удивительных свойств макромолекул является то, что α-спирали с левой и правой «резьбой» встречаются в живой природе с существенно разной вероятностью: макромолекул, «закрученных» вправо, почти нет. Асимметрию биологических веществ относительно зеркального отражения обнаружил в 1848 г. великий французский ученый Л. Пастер. Впоследствии выяснилось, что эта асимметрия присуща не только макромолекулам (белкам, нуклеиновым кислотам), но и организмам в целом. Как возникла преимущественная спиральность макромолекул и как она в дальнейшем закрепилась в ходе биологической эволюции — эти вопросы до сих пор являются дискуссионными и не имеют однозначного ответа.
Наиболее сложные и тонкие особенности структуры, отличающие один белок от другого, связаны с пространственной организацией белка, которую называют третичной структурой. Фактически речь идет о том, что спиралевидные цепочки аминокислотных остатков свернуты в нечто, напоминающее клубок ниток; В результате довольно длинные цепочки занимают сравнительно небольшой объем в пространстве. Характер свертывания в клубок отнюдь не случаен. Напротив, он однозначно определен для каждого белка. Именно благодаря третичной структуре белок способен выполнять свои уникальные каталитические, ферментативные функции, когда в результате целенаправленного захватывания реагентов осуществляется их синтез в сложные химические соединения, сравнимые по сложности с самим белком. Ни одна из химических реакций, осуществляемых белками, не может происходить обычным образом.
Кроме третичной структуры, белок может иметь четвертичную структуру; когда имеет место структурная связь между двумя или несколькими белками. Фактически речь идет об объединении нескольких «клубков» из полипептидных цепочек.
Нуклеиновые кислоты (от лат. nucleus — ядро) — высокомолекулярные органические фосфорсодержащие соединения, биополимеры. Полимерные формы нуклеиновых кислот называют полинуклеотидами. Цепочки из нуклеотидов соединяются через остаток фосфорной кислоты (фосфодиэфирная связь). Поскольку в нуклеотидах существует только два типа гетероциклических молекул, рибоза и дезоксирибоза, то и имеется лишь два вида нуклеиновых кислот — дезоксирибонуклеиновая (ДНК) и рибонуклеиновая (РНК). Нуклеиновые кислоты ДНК и РНК присутствуют в клетках всех живых организмов и выполняют важнейшие функции по хранению, передаче и реализации наследственной информации. Одна из основных аксиом биологии утверждает, что наследственная информация о структуре и функциях биологического объекта передается из поколения в поколение матричным путем, а носителями этой информации являются нуклеиновые кислоты.
Эти биополимеры на первый взгляд проще, чем белки. «Алфавит» нуклеиновых кислот состоит всего из четырех «букв», в роли которых выступают нуклеотиды — сахара-пентозы, к которым присоединено одно из пяти азотистых оснований: гуанин (Г), аденин (А), цитозин (Ц), тимин (Т) и урацил (У).
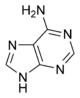 | 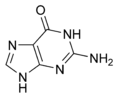 | 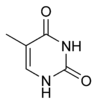 | 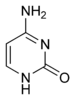 |
| Аденин | Гуанин | Тимин | Цитозин |
Рис. 2 Структуры оснований, наиболее часто встречающихся в составе ДНК
В рибонуклеиновой кислоте (РНК) сахаром является углевод рибоза (С5Н10О5), а в дезоксирибонуклеиновой кислоте (ДНК) — углевод дезоксирибоза (С5Н10О4), который отличается от рибозы только тем, что около одного из атомов углерода ОН-группа заменена на атом водорода. Три из указанных азотистых оснований — Г, А и Ц — входят в состав и РНК, и ДНК. Четвертое азотистое основание в этих кислотах разное — Т входит только в ДНК, а У— только в РНК. Связываются звенья нуклеотидов фосфодиэфирными связями остатка фосфорной кислоты Н3РО4.
Относительные молекулярные массы нуклеиновых кислот достигают значений 1500 000-2 000 000 и более. Вторичная структура ДНК была установлена методами рентгеноструктурного анализа в 1953 г. Р. Франклин, М. Уилкинсом, Дж. Уотсоном и Ф. Криком. Оказалось, что ДНК образуют спирально закрученные нити, причем азотистое основание одной нити ДНК связано водородными связями с определенным основанием другой нити: аденин может быть связан только с тимином, а цитозин — только с гуанином (рис. 3). Такие связи называются комплементарными (дополнительными). Отсюда следует, что порядок расположения оснований в одной нити однозначно определяет порядок в другой нити. Именно с этим связано важнейшее свойство ДНК — способность к самовоспроизведению (репликации). РНК не имеет двойной спиральной структуры и построена как одна из нитей ДНК. Различают рибосомную (рРНК), матричную (мРНК) и транспортную (тРНК). Они отличаются теми ролями, которые играют в клетках.
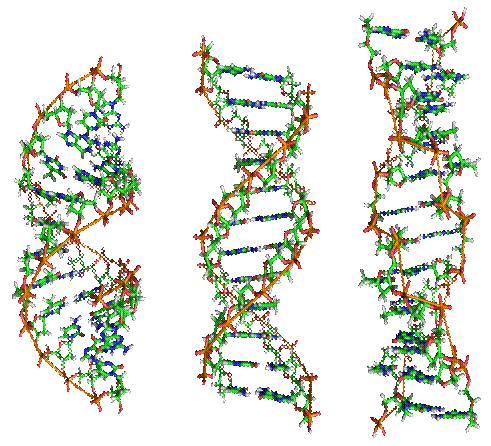
Рис. 3 Различные формы двойной спирали ДНК
Что же означают последовательности нуклеотидов в нуклеиновых кислотах? Каждые три нуклеотида (их называют триплетами или кодонами) кодируют ту или иную аминокислоту в белке. Например, последовательность УЦГ дает сигнал на синтез аминокислоты серин. Сразу возникает вопрос: сколько различных троек можно получить из четырех «букв»? Легко сообразить, что таких троек может быть 43 = 64. Но в образовании белков может участвовать всего 20 аминокислотных остатков, значит, некоторые из них можно кодировать разными тройками, что и наблюдается в природе.
Например, лейцин, серин, аргинин кодируются шестью тройками, пролин, валин и глицин — четырьмя и т. д. Это свойство триплетного генетического кода называется вырожденностью или избыточностью. Следует также отметить, что для всех живых организмов кодирование белков происходит одинаково (универсальность кодирования). В то же время последовательности нуклеотидов в ДНК не могут быть считаны иначе, как единственным способом (неперекрываемость кодонов).
 2015-04-23
2015-04-23 15265
15265








