Для решения задачи воспользуемся уравнением Менделе- ева – Клапейрона, применив его к конечному состоянию газа:
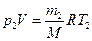 , (1)
, (1)
где m2 – масса гелия в баллоне в конечном состоянии; М – молярная масса газа; R – молярная газовая постоянная.
Из уравнения (1) выразим искомое давление:
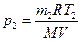 . (2)
. (2)
Массу m2 выразим через массу m1, соответствующую начальному состоянию, и массу m гелия, взятого из баллона:
m 2 = m1- m. (3)
Массу m1 найдём из уравнения Менделеева – Клапейро- на, применив его к начальному состоянию газа:
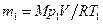 . (4)
. (4)
Подставляя выражение массы m1 в (3), а затем выражение m2 в (2), найдём
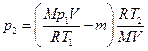 ,
,
или
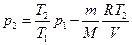 .
.
Произведя вычисления, получим
Р2 = 3,64·105 Па = 0, 364 МПа.
Пример 4. В сосуде объёмом V =5 л находится азот массой m =1,4 г при температуре Т = 1800 К. Найти давление газа, имея в виду, что при этой температуре h = 30% молекул диссоциировано на атомы.
 2015-05-14
2015-05-14 673
673







