Химическая металлизация ПП используется в качестве подслоя для нанесения основного слоя токопроводящего рисунка гальваническим способом при субтрактивном полуаддитивном методе или основного слоя при изготовлении плат аддитивным методом. Толщина слоя химической меди должна составлять 0,25 – 1,0 мкм, покрытие должно быть однородным, пластичным, хорошо сцепленным с диэлектриком.
Для придания диэлектрику способности к металлизации проводят такие подготовительные операции, как сенсибилизация и активация поверхности.
Сенсибилизация (от лат. sensibilis – чувствительный) имеет целью формирование на поверхности диэлектрика пленки ионов двухвалентного олова Sn2+, являющихся восстановителем для ионов активатора металлизации. Платы обрабатывают в растворе двухлористого олова и соляной кислоты в соотношении 1:4 в течение 5 – 7 мин и промывают в деионизованной воде. Образование гидроксида олова происходит по реакциям:
SnCl2 + Н2О = Sn(OH)Cl + HC1, Sn(OH)Cl + Н2О = Sn(OH)2 + НС1.
Электронно-микроскопические исследования показали, что гидроксид двухвалентного олова адсорбируется в виде отдельных участков размером порядка 10 нм на расстоянии
20 – 30 мкм друг от друга так, что им покрывается вся поверхность диэлектрика. Гидроксид двухвалентного олова обладает сильными восстановительными свойствами.
Активация поверхности диэлектрика проводится в растворах солей благородных металлов, преимущественно палладия, и способствует последующему осаждению меди. Активирующий раствор имеет следующий состав:
– 3,5 – 4,0 г/л PdCl2,
– 10 – 20 мл/л НС1,
– остальное – вода,
процесс осуществляют при температуре 40 – 50°С (рН = 3,5 – 0,5) в течение 5 – 7 мин.
Реакция восстановления палладия на диэлектрике:
Sn(OH)2 + PdCl2 = Pd + SnO2 + 2HC1,
в ионном виде: Sn2+ + Pb2+ = Sn4+ + Pb°,
на торцах контактных площадок:
Cu + PbCl2 = Pb + CuCl2.
На поверхности изоляционного материала вследствие адсорбции и восстановления палладия образуется тонкая сетка частиц размером порядка 10 нм. Связь частиц палладия с подложкой определяется их внедрением в поры диэлектрика, а также образованием ковалентных связей между металлом и материалом подложки. Для хорошего сцепления необходимо, чтобы на поверхности диэлектрика было не менее 1·10 - 6 кг/см2 палладия. Пленка палладия, образующаяся на торцах контактных площадок, является нежелательной, так как приводит к снижению прочности химически осажденной меди в результате образования гидридов палладия при захватывании палладием водорода. Кроме того, это приводит к образованию высокого и неравномерного переходного электрического сопротивления.
Химическое осаждение меди – окислительно-восстановительный процесс, который происходит вследствие восстановления ионов двухвалентной меди на активированных поверхностях из ее комплексных солей. Основными компонентами раствора химического меднения являются:
– 15–20 г/л сернокислой меди CuSO4 источника катионов Сu2+;
– 2 – 4 г/л солей никеля N1CI2 для большей прочности сцепления меди с диэлектриком;
– 10 – 15 г/л щелочи NaOH для создания рН = 10 – 13;
– 2 – 4 г/л Na2CO3 для увеличения скорости химического меднения и как буферная добавка;
– 4 – 16 г/л восстановителя – 33 %-го раствора формалина (СНОН);
– комплексообразователь – калий виннокислый как стабилизатор раствора – 50 – 60 г/л.
При введении формалина в раствор реакция восстановления меди при комнатной температуре становится автокаталитической. Процесс химического меднения представляет собой сумму электрохимических реакций катодного восстановления металла и анодного окисления восстановителя. Основная катодная реакция восстановления меди выражается уравнением:
Сu2++2НСОН + 4OH- → Сu + Н2 + 2НСОО- + 2Н2О.
Анодная реакция заключается в окислении формалина при рН = 12 – 13 и потенциале +0,80В. Время осаждения подслоя меди толщиной 0,5 мкм при температуре 20 °С составляет 15 – 20 мин. Для облегчения удаления водорода и лучшего омывания раствором отверстий малого диаметра процесс ведется с плавным покачиванием плат (8 – 10 качаний в минуту при амплитуде 50 – 100 мм).
Гальваническую металлизацию в производстве ПП применяют:
– для образования проводящего рисунка схемы с толщиной меди в отверстиях не менее 25 мкм;
– для предварительного увеличения тонкого слоя химической меди до толщины 5 – 8 мкм с целью последующего формирования рисунка схемы;
– для нанесения металлического резиста, например олово – свинец, толщиной 10 – 20 мкм либо специальных покрытий золотом, серебром толщиной 2 – 5 мкм.
Гальванический метод нанесения металлических покрытий был изобретен в 1837 г. в России электротехником Б.С. Якоби и заключается в том, что деталь, подлежащая покрытию, помещается в электролитно-водный раствор солей металла в качестве катода, а анодом является осаждаемый металл (медь). Необходимые для восстановления электроны поступают от внешнего источника постоянного тока. Под действием напряжения ионы металла движутся к катоду, присоединяют электроны и осаждаются на нем как нейтральные атомы (рис. 2.14.)
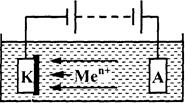
Рис. 2.14. Схема гальванической металлизации.
Реакция восстановления меди:
Сu2+ + 2е = Сu
Количественно процессы гальванической металлизации описываются первым законом Фарадея, согласно которому, масса выделяемого вещества при электролизе пропорциональна прошедшему количеству электричества I:
т = kIt,
где k – теоретический электрохимический эквивалент, пропорциональный молярной массе М и обратно пропорциональный химической валентности металла п (второй закон Фарадея): k = M/(Fn);
F – постоянная Фарадея: F ≈ 96 500 г/(А·с).
Для двухвалентной меди k = 1,186 г/(А·с), однако на практике теоретическое значение электрохимического эквивалента не достигается из-за побочных процессов, например осаждения водорода. Поэтому второй, не менее важной, характеристикой процесса гальванической металлизации является выход металла по току:
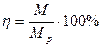
Время для нанесения покрытия заданной толщиной δ, считая, что масса
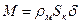
(где ρм – плотность металла; SK – площадь катода), определяется так:
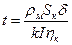
 2015-05-14
2015-05-14 2738
2738








