Вещества, молекулы которых в растворах или расплавах полностью или частично распадаются на ионы, называются электролитами. Растворы и расплавы электролитов проводят электрический ток.
Вещества, молекулы которых в растворах или расплавах на ионы не распадаются и электрический ток не проводят, называются неэлектролитами.
К электролитам относится большинство неорганических кислот, оснований и почти все соли, к неэлектролитам – многие органические соединения, например, спирты, эфиры, углеводы, и т.д.
Диссоциация – обратимый процесс: параллельно с диссоциацией протекает обратный процесс соединения ионов (ассоциация). Поэтому при написании уравнений реакции диссоциации электролитов в особенности в концентрированных растворах ставят знак обратимости 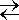 . Например, диссоциацию хлорида калия в концентрированном растворе следует записывать в виде.
. Например, диссоциацию хлорида калия в концентрированном растворе следует записывать в виде.
КС1 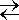 К+ + С1–.
К+ + С1–.
Дано:
m(смеси) = 540 мг
ω(примеси) = 0,4
V(H2) =?
n(соли) =?
Решение:
m(Al) = m(смеси) • ω(Al) = m(смеси) • (1 - ω(примеси))
m(Al) = 540 • (1 – 0,4) = 324 мг
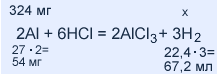
M(Al) = 27 мг / ммоль
324 / 54 = х / 67,2; х = (324 •67,2): 54 = 403 мл водорода;
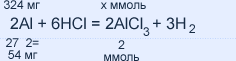
324 / 54 = х / 2; х = 12 ммоль соли хлорида алюминия AlCl3Ответ: V(H2) = 403 мл; n(AlCl3) = 12 ммоль.
Билет № 17:
Реакции, протекающие в растворах между электролитами, называются реакциями ионного обмена. (реакции ионного обмена – это реакции между ионами, образовавшимися в результате диссоциации электролитов).
Реакции обмена в растворах электролитов протекают в направлении связывания ионов.
При взаимодействии гидроксида натрия с соляной кислотой образуются хлорид натрия и малодиссоциирующее вещество вода:
NaOH + HCl = NaCl + H2O
Na+ + OH- + H+ + Cl- = Na+ + Cl- + H2O
OH- + H+ = H2O
При взаимодействии гидроксида натрия с раствором сульфата меди(II) образуются сульфат натрия и нерастворимое основание – гидроксид меди(II):
2NaOH + CuSO4 = Na2SO4 + Cu(OH)2?
2Na+ + 2OH- + Cu2+ + SO42- = 2Na+ + SO42- + Cu(OH)2?
2OH- + Cu2+ = Cu(OH)2?
При взаимодействии азотной кислоты с карбонатом калия образуются нитрат калия, вода и углекислый газ:
2HNO3 + K2CO3 = 2KNO3 + H2O + CO2#
2H+ + 2NO3- + 2K+ + CO32- = 2K+ + 2NO3- + H2O + CO2#
2H+ + CO32- = H2O + CO2#
Итак, реакции ионного обмена протекают до конца, если: 1) образуется осадок; 2) выделяется газ; 3) образуется малодиссоциирующее вещество – вода.
Если в растворах нет таких ионов, которые могут связываться между собой с образованием осадка, газа или воды, то реакция является обратимой, например, при взаимодействии растворов хлорида калия и нитрата натрия не происходит связывания ионов:
KCl + NaNO3 D KNO3 + NaCl
K+ + Cl- + Na+ + NO3- D K+ + NO3- + Na+ + Cl-
C7H16+11O2=7CO2+8H2O
n(C7H16)=10г: 100г/моль=0,1моль
Составляем пропорцию, где
n(CO2)=0.7 моль
n(H2O)=0,8 моль
Находим объем Углекислого газа
V(CO2)=0,7 моль * 22,4 л/моль= 15,68л
Теперь находим массу воды
m(H2O)=0.8 моль * 18 г/моль =14,4г
Билет № 18.
Ковалентной связью называется химическая связь между двумя атомами за счет образования общей электронной пары. Ковалентная связь может быть неполярной — между двумя атомами с одинаковой электроотрицательностью, т.е. в простых веществах, и полярной — между атомами, электроотрицательность которых различается, т.е. в сложных веществах.
Рассмотреть образование ковалентной неполярной связи удобно на примере молекулы водорода, образующейся при соединении двух атомов водорода, каждый из которых имеет по одному неспаренному электрону:
H• + •H → H: H
При этом внешняя электронная оболочка получает недостающий электрон, становится завершенной.
Такое состояние характеризуется меньшей энергией, более устойчиво. Вот почему для разрыва ковалентной связи требуется затратить энергию (такое же количество энергии выделяется при ее образовании).
В структурных формулах ковалентная связь изображается черточкой, тогда молекула водорода будет выглядеть так: H–H
Еще раз обращаем Ваше внимание, что ковалентной называется двухэлектронная двухцентровая связь, когда два электрона находятся на общей орбитали двух атомов. Поэтому к ней, строго говоря, не относятся случаи, когда электроны находятся на орбиталях трех или более атомов или когда общая связь образована более чем двумя электронами (в 10–11 классах будет изучаться бензол, в молекуле которого 6 электронов образуют одну общую связь).
Ковалентная полярная связь образуется в молекуле хлороводорода:
....
H· + ·Cl: → H:Cl:
·· ··
Хлор как более электроотрицательный элемент смещает к себе общую электронную пару, в результате на нем образуется частичный отрицательный заряд, а на водороде — частичный положительный:
Hδ+–Clδ−
Ковалентная связь может возникать не только при объединении двух орбиталей, содержащих по одному неспаренному электрону. Один атом может предоставить электронную пару, а второй — свободную орбиталь. Такая ковалентная связь называется донорно-акцепторной.
Например, в ионе аммония протон присоединяется к молекуле аммиака за счет образования донорно-акцепторной связи. Азот выступает донором, а протон (водород) — акцептором электронной пары:
H+ +:NH3 → NH4+
Ионную связь можно рассматривать как крайний случай ковалентной полярной связи, когда электроны практически полностью переходят от одних атомов к другим с образованием ионов.
Таким образом, ионная связь образуется за счет сил электростатического притяжения между ионами (притягиваются противоположные заряды).
Примером ионной связи будет хлорид натрия Na+ [:Cl:] −
Ионная связь характерна для соединений элементов, электроотрицательности которых различаются очень сильно, например щелочных металлов с галогенами.
Сходство с ковалентной связью заключается в том, что сложно провести резкую грань между ковалентной полярной и ионной связью, мнения разных авторов на этот счет могут различаться.
Различие ионной и ковалентной связи в том, что ионная сильнее поляризована, вплоть до полного перехода электронной пары к более электроотрицательному элементу.
1. Ионная — в узлах кристаллической решетки расположены положительные и отрицательные ионы. Характерна для веществ с ионной связью: соединений галогенов с щелочными металлами (NaCl), щелочей (NaOH) и солей кислородсодержащих кислот (Na2SO4).
2. Атомная — в узлах кристаллической решетки атомы, связанные ковалентными связями: алмаз, кремний.
Вещества с ионными и атомными кристаллическими решетками обладают высокими твердостью и температурой плавления.
3. Молекулярная кристаллическая решетка образована молекулами, связанными слабыми межмолекулярными взаимодействиями, поэтому такие вещества непрочные, легкоплавкие (лёд, сера), зачастую возгоняются, т.е. при нагревании испаряются, минуя жидкую фазу, как сухой лёд CO2, йод I2
4. Металлическая кристаллическая решетка характерна для металлов, например, Fe
 2015-05-30
2015-05-30 1084
1084
