Если для приготовления раствора используются кристаллогидраты (напр., медный купорос CuSO4×5H2О или глауберова соль Na2SO4×10H2О и так далее), тогда при приготовлении раствора необходимо учитывать воду, которая входит в состав кристаллогидрата.
Если m(kr) масса кристаллогидрата в граммах,
m(B) масса безводного компонента кристаллогидрата в граммах,
M(kr) молекулярная масса кристаллогидрата,
M(B) молекулярная масса безводного кристаллогидрата, тогда:
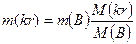 ;
; 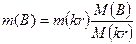
Задача. Ск. надо взять медного купороса, чтобы приготовить 500 г 16%
раствора сульфата меди CuSO4. M(kr) = 250, M(CuSO4) = 160.
Решение: для приготовления 500 г 16% раствора соли надо взять х(г) соли:
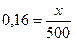 х = 80г.
х = 80г. 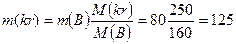 г. Ответ: 125 г.
г. Ответ: 125 г.
Задача. Какое количество медного купороса (CuSO4•5H2O) вступило в реакцию с едким натром, если при этом получено 0,196 г гидроксида меди.
Решение: из уравнения реакции видно, что в осадок выпадает такое же количество гидроксида меди, как и количество медного купороса, которое вступило в реакцию: CuSO4 + 2NaOH = Cu(OH)2 + Na2SO4. 0,196г Cu(OH)2 это 0,196/98 = 0,002 моля гидроксида меди, а это 0,002×250 = 0,5г медного купороса.
 2015-06-05
2015-06-05 5056
5056








