1)Отличие: Ферменты обладают высокой специфичностью.
-ферментативная реакция происходит при t 37 постоянном атмосферным давлением и физиологическом значении.
-Скорость фермент. ре-ции выше чем у неорганических катализаторов.
Особенности при t инактивируется.
- при гидролизе распад на АК как и белки.
- Синтез из АК по ген.коду искусственных белков,обладающих каталитическими свойствами,присущими натуральным ферментам.
Скорость реакции зависит от t pH среды.
Скорость реакции ферментов опред изменением кол-ва субстрата или продукта за ед.времени.
Скорость ферментативной реакции зависит от каталитической активности фермента.
2) Зависимость V от кол. фермента.
3)НАДН (измен в бенз. Кольцо) в книге есть.(308)
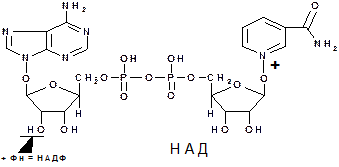
Функционирует как КоQ редуктаза
Способность промежуточного переносчика ионов водорода (Н) за счет амидоникотиновый кислоты,(происходит обратимое гидрирование.)
4)Заболевание диагностируется по изменению активности ферментов.
Синдром Катахара- недостаток или отсутствие каталазы.
Хронический панкреатит-снижение ур-ня панкреатической липазы.
Рахит-повышение щелочной фосфатазы.
Заболевание моче выдел.системы (уреаза)
5)Биологическое Окис.- распад органических веществ в живых тканях сопровождающая потреблением кислорода и выделением СО2 и Н2О и образ биологических видов энергии.
-В живой природе протекает при низкой t и с участием воды.
-Окисляется глюкоза в живых клетках (внутренний мембране митохондрии) и основная функция энергетическое обеспечение метоболизма.
-окислительное фосфолирование -один из важнейших компонентов клеточного дыхания, приводящего к получению энергии в виде АТФ из АДФ с Н3РО4.
+ комплекс 1 +
НАДН + Н + Q ===è HAД + QH2
Н +2е
3+ комплекс 3 + 2+
QH2 + 2e (Fe) =====è Q +2 H +2 e (Fe)
_ 2+ комплекс 4 _ 3+ 4-
4 e (Fe) +Q ==è 4e (Fe) + О2
_ цитохром
_ оксидаза
О2 + 4 е +4 Н ====è 2 H2O
Комплекс 1 НАДН дегидрогеназа Ф-ует QH2 редуктаза
Комплекс 3 Цитохромы в и с1 Ф-ует QH2 дегидрогеназа
Комплекс 4 Цитохромы а и а3 Ф-ует цитохромоксидаза
Комплекс 2 Сукцинатдегидрогеназа.
 2015-06-26
2015-06-26 849
849








