К а = [H3O+][[B]/[HB+]
или
р К а = рН + lg([HB+]/[B]) (А)
Для основания можно аналогично записать константу основности:
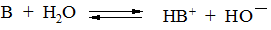
К b = [HO–][HB+]/ [B]
или
р Kb = рОН – lg([HB+]/[B]) (В)
Если сложить правые и левые части уравнений (А) и (В), то получим:
р К а + р Kb = рН + рОН = 14
Сумма рН + рОН соответствует автопротолизу воды, как амфотерного соединения, для которого кислотно-основное равновесие запишется как
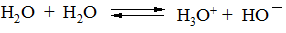
 К а = [H3O+][HO ]/[H2O]
К а = [H3O+][HO ]/[H2O]
или
р К а = рН + рОН + lg[H2O]
Зная значение концентрации воды ([H2O] ≈ 55 моль/л), можно рассчитать, что для воды
р К а = 14 + lg[55] = 15.74
 2015-06-24
2015-06-24 846
846








