Вычислите температуры кристаллизации, и кипения раствора с массовой долей сахара C12H22O11 5 %.
Решение.
При растворении в растворителе нелетучего вещества давление пара растворителя над раствором уменьшается, что вызывает повышение температуры кипения раствора и понижение температуры его замерзания по сравнению с чистым растворителем. При этом, согласно закону Рауля, повышение температуры кипения (Dtкип.) и понижение температуры замерзания (Dtзам.) раствора пропорционально моляльной концентрации раствора:
DТк = Э · Cm, DТз = К · Сm.
Здесь Cm - моляльная концентрация раствора (число молей растворенного вещества в 1000 г растворителя); Э - эбуллиоскопическая константа растворителя, град; К - криоскопическая константа растворителя, град.
Так как молярная концентрация 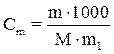 ,
,
где m - масса растворенного вещества, г; M - молярная масса растворенного вещества, г/моль; m1 - масса растворителя, г, то формулы закона Рауля можно записать следующим образом:
DТк = 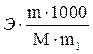 , DТз =
, DТз = 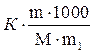 .
.
Эти формулы позволяют определить температуры замерзания и кипения растворов по их концентрации, а также находить молекулярную массу растворенного вещества по понижению температуры замерзания и повышению температуры кипения раствора.
Для воды криоскопическая константа (К) и эбуллиоскопическая константа (Э) соответственно равны 1,86 и 0,52 град. Молярная масса сахара 342 г/моль. Рассчитаем понижение температуры кристаллизации раствора с массовой долей сахара 5 %:
DТз = 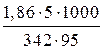 = 0,29 °С.
= 0,29 °С.
Вода кристаллизуется при 0 °С, следовательно, температура кристал-лизации раствора будет 0 - 0,29 = - 0,29 °С.
Из формулы рассчитываем повышение температуры кипения этого раствора:
DТк = 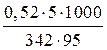 = 0,06 °С.
= 0,06 °С.
Вода кипит при 100 °С. Следовательно, температура кипения этого раствора будет 100 + 0,06 = 100,06 °С.
 2015-06-24
2015-06-24 1457
1457