Составьте молекулярные и ионные уравнения реакций, протекающих между веществами:
1. AgNO3 + FeCl3 ®
2. Na2S + HCl ®
3. HCN + KOH ®
4. Zn(OH)2 + NaOH ®
Решение.
Реакции в растворах электролитов протекают между ионами, их записывают с помощью ионных уравнений. Большинство этих реакций относят к типу обменных, и сущность их сводится к соединению ионов в молекулы новых веществ. Обязательным условием протекания реакций обмена между электролитами в растворах является образование:
малорастворимых веществ,
слабых электролитов,
газообразных веществ,
комплексных ионов.
При составлении ионного уравнения все перечисленные выше вещества пишутся в виде молекул, а сильные электролиты - в виде ионов, независимо от того, в левой или правой частях уравнения они находятся.
Распишем реакции, приведенные в условии задачи в молекулярном и ионном виде.
Молекулярное уравнение:
1. 3AgNO3 + FeCl3 = 3AgCl¯ + Fe(NO3)3.
Полное ионное уравнение:
3Ag+ + 3NO 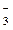 + Fe3+ + 3Cl- = 3AgCl¯ + 3Fe3+ + 3NO
+ Fe3+ + 3Cl- = 3AgCl¯ + 3Fe3+ + 3NO 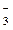 .
.
Если из правой и левой частей уравнения исключить одинаковые ионы, то получим краткое ионное уравнение, выражающее суть данной реакции.
Краткое ионное уравнение:
3Ag+ + 3Cl- = 3AgCl¯.
Подобным образом расписываем остальные реакции.
2. Na2S + 2HCl =2NaCl + H2S.
2Na+ + S2– + 2H+ + 2Cl– =2Na+ + 2Cl– + H2S.
2H+ + S2– = H2S.
3. HCN + KOH = KCN + H2O.
HCN + K+ + OH- = K+ + CN- + H2O.
HCN + OH- = CN- + H2O.
4. Zn(OH)2¯ + 2NaOH = Na2[Zn(OH)4].
Zn(OH)2¯ + 2Na+ + 2OH- = 2Na+ + [Zn(OH)4]2-.
Zn(OH)2¯ + 2OH- = [Zn(OH)4]2-.
 2015-06-24
2015-06-24 2535
2535
