Устойчивые к затоплению (аноксии) растения, т.е. растения второй группы, могут выдерживать его лишь ограниченный период времени. При затоплении они синтезируют АТФ за счет анаэробного метаболизма. В это время ростовые процессы в корне (удлинение клеток) подавляются. Общая скорость синтеза белка снижается, а в экспрессии генов происходят заметные изменения. Проростки устойчивых к затоплению сортов кукурузы могут выдерживать аноксию на протяжении 3 — 5 дней в зависимости от генотипа и возраста растений. Устойчивость к затоплению возрастает, если молодые растения предварительно подвергнуть гипоксической обработке. Гипоксия активирует гликолиз, а также способствует формированию боковых корней, несущих аэренхиму в коре.
У чувствительных растений (первая группа), как и у резистентных, скорость гликолиза в ответ на затопление возрастает, однако они быстро повреждаются, поскольку активирование гликолиза у них приводит к закислению цитоплазмы. Скорость синтеза белка в этих условиях снижается, митохондрии подвергаются деструктивным изменениям, процессы деления и растяжения клеток подавляются, нарушается транспорт ионов, а клетки корневой меристемы отмирают. В условиях аноксии у чувствительных растений аэренхима не образуется. Они способны выдержать затопление на протяжении не более суток. Таким образом, непродолжительное затопление активирует в растениях гликолитический путь, независимо от степени их устойчивости к дефициту О2. Простые сахара, субстраты гликолиза, транспортируются из листьев по флоэме в затопленные органы. В затопленных колеоптилях риса происходит гидролиз крахмала, дополнительно снабжающий растения гликолитическими субстратами.
В результате гликолиза 6-углеродная молекула глюкозы расщепляется на две 3-углеродные молекулы пировиноградной кислоты (ПВК); образуются две молекулы АТФ, а НАД+ восстанавливается до НАДН (рис. 8.30).
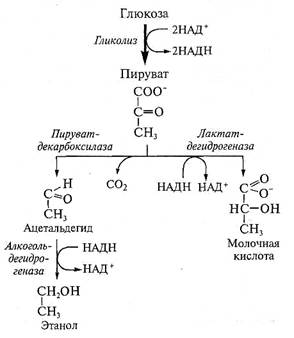
Рис. 8.30. Образование этанола и молочной кислоты из конечного продукта гликолиза — пировиноградной кислоты в условиях кислородного дефицита.
Образование обоих продуктов сопряжено с регенерацией НАД+. Образование этанола не приводит к изменениям рН цитозоля, тогда как образование молочной кислоты вызывает ацидоз
Чтобы гликолиз продолжался в отсутствие митохондриального дыхания, необходимо постоянно регенерировать НАД+. Регенерация осуществляется в последующих реакциях ферментации. Существует два основных пути превращений ПВК, ведущих к регенерации НАД+. Первый путь связан с декарбоксилированием ПВК и последующим восстановлением продукта декарбоксилирования — ацетальдегида. В этих превращениях участвуют два фермента: пи-руватдекарбоксилаза (ПВД) и алкогольдегидрогеназа (АДГ) соответственно. Конечным продуктом этих двух реакций является этиловый спирт. Второй путь осуществляется лактатдегидрогеназой
(ЛДГ), которая восстанавливает ПВК до молочной кислоты (МК). Доли двух путей в превращениях ПВК различны в зависимости от вида растения, его устойчивости к недостатку кислорода, ткани, а также от продолжительности и степени О2-дефицита. Оба пути ведут к регенерации НАД+, однако образование молочной кислоты связано с нежелательным явлением — закислением цитозоля, тогда как при образовании этилового спирта рН цитозоля не изменяется. Говоря иначе, накопление молочной кислоты может вызвать вторичные токсические эффекты в результате ацидоза цитоплазмы. В связи с этим можно считать, что важная роль в устойчивости растений к О2-дефициту принадлежит способности клетки предотвращать закисление цитозоля.
Согласно гипотезе Дэвиса—Робертса, регуляция рН цитозоля при анаэробном метаболизме зависит от соотношения активностей лактатдегидрогеназы и пируватдекарбоксилазы (см. рис. 8.30). Образующаяся при гликолизе ПВК превращается в МК в реакции, катализируемой ЛДГ. Этот фермент имеет оптимум активности при физиологических значениях рН цитоплазмы. При образовании МК цитоплазма закисляется. По мере снижения рН ЛДГ прогрессивно ингибируется, тогда как ПДК, включенная в путь образования этилового спирта, активируется, поскольку ее оптимум активности смещен в кислую область. Таким образом, аккумуляция МК стимулирует превращение ПВК в ацетальдегид, который далее восстанавливается алкогольдегидрогеназой до этилового спирта. В отличие от МК молекула этилового спирта не несет заряда и может легко диффундировать через плазмалемму в среду. В результате включения пути, ведущего к образованию этилового спирта, рН цитозоля стабилизируется на уровне слабокислых значений. О таком регуляторном механизме свидетельствуют эксперименты с трансгенными растениями табака со сверхэкспрессией пируватдекарбоксилазы. Повышенная активность ПДК у трансформантов по сравнению с растениями дикого типа стимулировала ферментацию этанола и приводила к подавлению образования МК в цитозоле. Роль ферментации этанола в предотвращении ацидоза и в обеспечении устойчивости растений к недостатку О2 была продемонстрирована на мутанте кукурузы, дефицитном по АДГ. Нормальные растения кукурузы характеризуются резистент-ностью к затоплению. Мутант, дефицитный по алкогольдегидрогеназе, которая не требуется для роста в аэробных условиях, оказался более чувствительным к затоплению, чем растения дикого типа. В анаэробных условиях накопление ацетальдегида в его клетках и закисление цитоплазмы было сильнее, чем у растений дикого типа. Таким образом, резистентные к затоплению растения обладают способностью переключать ферментацию молочной кислоты, приводящей к ацидозу, на ферментацию этилового спирта — нейтрального соединения. Чувствительные к затоплению растения, например горох, хотя и накапливают этанол в условиях О2-дефицита, не способны избежать закисления цитоплазмы. У них ферментация этанола осуществляется параллельно с ферментацией МК.
При физиологических значениях рН цитозоля значительная часть образующейся МК находится в анионной форме и вследствие этого не может транспортироваться через плазмалемму. При ацидозе доля недиссоциированных, т. е. способных пересекать мембрану, молекул молочной кислоты возрастает и она может диффундировать из цитозоля наружу. Считается, что выход образующейся при дефиците О2 МК в наружную среду является одним из механизмов,
останавливающих закисление цитоплазмы. Полагают, что клетки толерантных к дефициту О2 растений по сравнению с клетками чувствительных растений более эффективно экспортируют МК наружу.
 2015-06-26
2015-06-26 1523
1523
