Гидролиз солей. Расчет рН растворов солей
Цель работы: изучение влияния различных факторов на гидролиз.
Задачи: 1) выяснить возможности использования индикаторов для определения наличия и типа гидролиза солей; 2) освоить методику рассмотрения процессов гидролиза солей всех типов.
Реактивы и оборудование: 1)HNO3, (конц.); 2) 0,5н. растворы CH3COONa, Bi(NO3)3, A12(SO4)3, Na2CO3; 3) индикаторы: тимоловый синий, фенолфталеин; 4) штативы с пробирками, 5) пробиркодержатель, 6) водяная баня.
Химическое обменное взаимодействие ионов растворенной соли с молекулами воды, приводящее к образованию слабодиссоциирующих продуктов (кислот, оснований, кислых анионов, основных катионов) и сопровождающееся изменением рН среды, называется гидролизом соли. Из определения следует, что гидролизу подвергаются не все соли: если взаимодействие между ионами соли и молекулами воды не происходит, то гидролиз отсутствует:
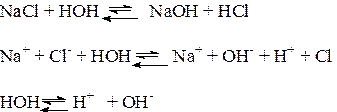
Практически идет обратная реакция - нейтрализация, с образованием слабого электролита Н2О.
В этом состоит сходство гидролиза с другими обменными реакциями электролитов - кислот, оснований, солей. Отличия реакций солей с водой от их реакций с кислотами и щелочами связаны с электролитическими особенностями воды. Как и кислоты, вода образует при диссоциации Н+ - ионы и как щелочи – ОН- - ионы. Но и те и другие присутствуют в чистой воде в очень небольшой концентрации (10-7 моль/л). Поэтому гидролиз ионов соли происходит, во-первых, обратимо, кроме отдельных случаев, во вторых, для многозарядных ионов - ступенчато. При составлении уравнений реакций гидролиза следует помнить, что во избежание распространенной ошибки нельзя использовать более одной молекулы воды на один ион соли:
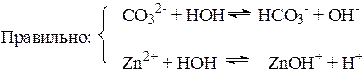
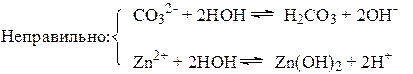
Известны три типичных случая:
1) Соли, образованные слабым основанием и сильной кислотой, гидролизуются по катиону, который связывает ОН- - ионы воды; в растворе накапливаются ионы водорода Н+, и раствор приобретает кислую реакцию среды, рН<7.
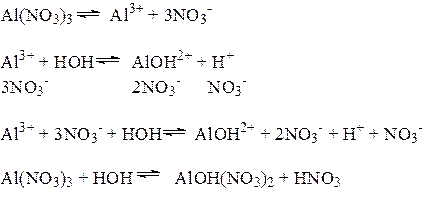
Характер гидролиза: частичный, обратимый, ступенчатый.
2) Соли, образованные сильным основанием и слабой кислотой, гидролизуются по аниону, который связывает Н+-ионы воды; в растворе накапливаются ОН- ионы, создавая щелочную среду, рН>7.

Характер гидролиза: частичный, обратимый.
3) Соли, образованные слабым основанием и слабой кислотой, гидролизуются по катиону и по аниону
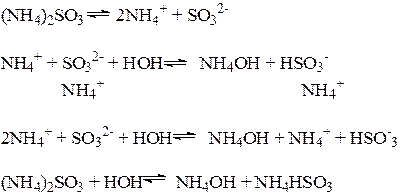
Кдисс. (HSO3-) = 6,3 × 10-8 < Кдисс (NH4OH) = 1,8 × 10-5
Анион SO32- - гидролизуется сильнее, Н+ - ионов связывается больше, чем ОН- -ионов. Среда раствора слабощелочная.
Характер гидролиза: полный, обратимый, ступенчатый.
Количественно гидролиз характеризуют степенью гидролиза (h) и константой гидролиза (Кг). Степень гидролиза - это отношение концентрации соли, подвергшейся гидролизу (Сг) к общей концентрации соли в растворе (См)
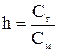 или
или 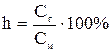
1) Для соли, гидролизующейся по аниону:

Константа равновесия, описывающая этот процесс, равна
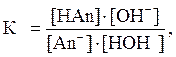
где [HOH]» CН2О = const, так как на гидролиз соли расходуется незначительное количество воды;
Если умножить левую и правую части уравнения на [H2O], то в левой части уравнения окажутся две постоянные К и [H2О]. Произведения двух постоянных называются константой гидролиза (Кг):
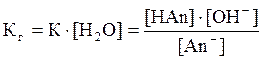
Если в уравнении (6) числитель и знаменатель дроби умножить на одну и ту же величину [H+], то в числителе можно выделить ионное произведение воды:
Кw = [OH-]∙[H+]
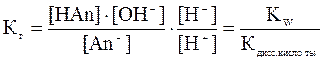 ,
,
где 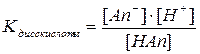 .
.
Концентрация [OH-] = h × Cм, где h – степень гидролиза, которая связана с константой гидролиза уравнением
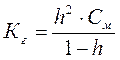 .
.
Так как степень гидролиза очень мала, то 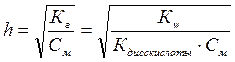 .
.
[OH-] = h × Cм = 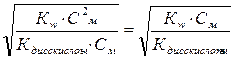
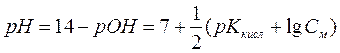 )
)
2) Для соли, гидролизующейся по катиону:
Kt+ + HOH «KtOH + H+
Константа равновесия равна
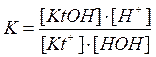
Константа гидролиза в этом случае равна
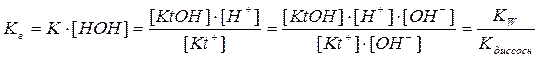 ,
,
Где 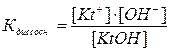
Концентрация H+ равна [H+] = h × Cм
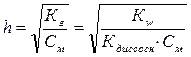 ,
,
[H+] = h × Cм = 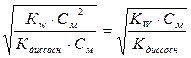
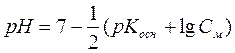
Числовые значения констант диссоциации кислых анионов и основных катионов значительно меньше констант диссоциации соответствующих кислот и оснований. Поэтому гидролиз идет преимущественно по I ступени:
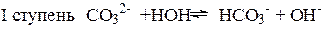
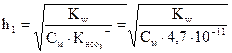
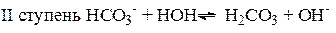
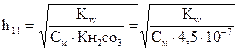
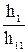 =
= 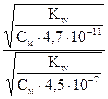 » 100
» 100
Гидролиз аниона СО32- по первой ступени превышает гидролиз по второй ступени примерно в 100 раз.
Соли третьего типа гидролизуются наиболее сильно. Если кислота и основание, образующие соль, не только слабые электролиты, но и малорастворимы, или неустойчивы и разлагаются с образованием летучих продуктов, то происходит полный, необратимый гидролиз:
Cr2S3 + 6HOH ® 2Cr(OH)3 ¯ + 3H2S
По этой причине не могут быть получены в водных растворах такие соли, как Cr2S3, A12S3, A12(CO3)3, Fe2(CO3)3, Cr2(CO3)3 и др.
Пример:
Cr2(SO4)3 + 3Na2S ® Cr2S3 + 3Na2SO4
+
Cr2S3 + 6HOH ® 2Cr(OH)3 ¯ + 3H2S
________________________________________
Cr2(SO4)3 + 3Na2S + 6HOH ® 2Cr(OH)3 ¯ + 3H2S + 3Na2SO4
2Cr3+ + 3SO42- + 6Na+ + 3S2- + 6HOH ® 2Cr(OH)3¯ + 3H2S + 6Na+ + 3SO42-
2Cr3+ + 3S2- + 6HOH ® 2Cr(OH)3¯ + 3H2S
Совместное присутствие ионов Сг3+ и S2- усиливает их гидролиз, в результате вместо сульфида хрома образуются гидроксид хрома и сероводород, что может быть легко доказано экспериментально.
 2015-08-13
2015-08-13 3965
3965








