
2) Совместное решение графическим методом уравнений материального и теплового балансов для реакции A→R, ∆H>0. Адиабатический РИС.
Рассмотрим решение математической модели для адиабатического РИС.
Химический реактор – основной аппарат любого химического процесса:
1) он определяет экономическую эффективность всего технологического процесса
2) определяет конструктивные особенности процесса
3) определяет технические показатели
4) определяет эксплуатационные характеристики.
Реакторы смешения – это емкостные аппараты с перемешиванием механической мешалкой или циркуляционным насосом.
Для идеального смешения характерно абсолютно полное выравнивание всех характеризующих реакцию параметров по объему реактора.
Адиабатический режим характеризуется полным отсутствием теплообмена с окружающей средой (qтеплообм=0). В этом случае вся теплота химической реакции полностью расходуется на нагрев или охлаждение реакционной смеси. Для стационарного адиабатического режима: |Qвх - Qвых|=|Qхр|.
Рассмотрим простую необратимую эндотермическую реакцию: A→(K)R
1. Кинетическое уравнение: WrA=k*CA
2. Уравнение материального баланса: τср=V/υ=(CA0 – СА)/WrA
По определению степени превращения хА=(CA0 – СА)/ CA0,
тогда CA0 – СА=хА*СА0.
Тогда УМБ: τср=V/υ=CA0*хА/WrA
3. Уравнение теплового баланса в общем виде:
Qвх - Qвых± Qхр± Qто=Qнак
В стационарном режиме работы реактора: Qвх - Qвых± Qхр± Qто=0
Так как в адиабатическом реакторе Qто-0, то |Qвх - Qвых|=|Qхр|
ρ*Cp*υ(T0-T)-∆H*WrA*V=0
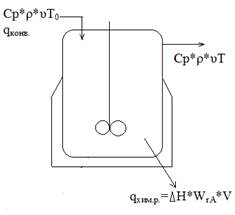
Решение:
1. τср= CA0*хА/WrA= CA0*хА/ k*CA
По определению степени превращения: СА=СА0(1-хА)
Тогда τср== CA0*хА/ k*CA== CA0*хА/ [k*СА0(1-хА)}
τср=xA/[K(1-xA)] → xA=1/[1+1/(K* τср)]
2.Согласно уравнению теплового баланса: ρ*Cp*υ(T0-T)-∆H*WrA*V=0
Подставим в него кинетическое уравнение: ρ*Cp*υ(T0-T)-∆H* k*CA *V=0
СА=СА0(1-хА)
Выразим степень превращения: xA=(Cp*ρ/CA0*∆H)*(T0-T)
Зависимость между степенью превращения и Т является линейной. Эта прямая линия пересекает ось температур в точке Т=Т0:
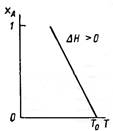
Если принять хА=1 (т.е. реакция прошла до конца), то получим
Т0 – Тх=1=∆Тад=Cp*ρ/CA0*∆H.
Величина ∆Тад – максимальное изменение температуры реакционной смеси, возможное в адиабатических условиях, или адиабатическое изменение температуры.
Тогда: xA=(1/∆Tаб.)*(T0-T) (1) – первое уравнение математической модели
второе уравнение представляет собой уравнение материального баланса:
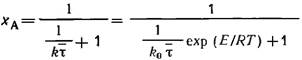 (2)
(2)
Возможно лишь графическое решение.
эндотермический реактор - ∆Н>0
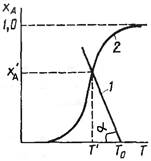
Рис. Уравнения теплового (1) и материального (2) балансов для адиабатического РИС при проведении в нем необратимой эндотермической реакции.
tgα= -1/∆Тадиабат.
tgα<0
Решение системы уравнений материального и теплового балансов представляет точку (хА’, T’) пересечения графиков функций (1) и (2).
Физико-химические основы процесса синтеза аммиака. Выбор технологического режима (температура, давление, концентрации компонентов, объемная скорость). Технологическая схема процесса.
Аммиак – ключевой продукт различных азотсодержащих веществ, применяемых в промышленности и сельском хозяйстве. Аммиак используется для получения азотной кислоты, полимерных материалов, в холодильной технике, для производства минеральных удобрений.
Состав аммиака был установлен Бертолле в 1784 году. Аммиак – NH3 – основание, умеренно сильный восстановительный агент и эффективный комплексообразователь.
NH3- газ с резким запахом.
Тконд= -33,5ᵒС
Тплавл= -77,8ᵒС
Растворимость: в 1л воды растворяется 700 л NH3
С воздухом аммиак образует взрывчатую смесь в интервале (15-27%)NH3
Синтез аммиака из элементов осуществляется по уравнению реакции: N2+3H2↔2NH3+Q – обратимая, экзотермическая.
Согласно принципу Ле-Шателье при нагревании равновесие смещается влево, в строну уменьшения выхода аммиака. Реакция синтеза аммиака протекает с уменьшением объема. Значит для интенсификации процесса получения аммиака необходимо: t↓ (420-550 ᵒС) и p↑ 320 атм, катализатор Fe.
Синтез аммиака протекает с заметной скоростью только в присутствии катализатора, причем твердого катализатора (железо). Гетерогенно-каталитический процесс синтеза аммиака имеет сложный механизм:
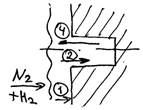
1) внешняя диффузия N2 и Н2 к поверхности катализатора;
2) Диффузия внутри пор катализатора
3) Химическая реакция на поверхности катализатора
3.1 Абсорбция на активных центрах Ϭ катализатора
N2+2Ϭ→2NϬ
H2+2Ϭ→2HϬ
3.2 Взаимодействие поверхностных комплексов:
NϬ+HϬ→NHϬ+Ϭ (NHϬ - имид)
NHϬ+ HϬ→NH2Ϭ+Ϭ (NH2Ϭ - амид)
NH2Ϭ+HϬ→NH3Ϭ+Ϭ (NH3Ϭ - аммиак)
3.3 десорбция NH3 с поверхности катализатора
NH3Ϭ→ NH3+Ϭ
4) Диффузия NH3 в порах катализатора
5) Диффузия NH3 через пограничную газовую пленку в газовый поток.
Лимитирующая стадия – хемосорбция азота (диффузия внутри пор катализатора).
Скорость обратимой реакции получения аммиака из элементов на большинстве катализаторов описывается уравнением Темкина-Пыжева:
w= dрNH3/dτ=k1*рN2*(р1,5 H2/рNH3)-k2*(рNH3/р1,5Н2)
Скорость реакции синтеза аммиака зависит от температуры, давления и состава реакционной смеси. Оптимальными считают такие значения указанных параметров, при которых скорость процесса максимальна.
Из этого уравнения видно, что скорость прямой реакции синтеза пропорционально р1,5, а скорость обратной – р0,5. Очевидно, что с ростом давления скорость процесса увеличивается.
С ростом давления увеличивается расход электроэнергии, при понижении давления снижается расход энергии, но увеличиваются размеры аппаратов. Для определения оптимального давления синтеза была использована комплексная математическая модель агрегата синтеза аммиака. В качестве критерия оптимизации – приведенные затраты.
На основании анализа определено, что наиболее эффективным является давление около 30 МПа.
Особенности:
1) высокое давление
2) наличие циркуляционного контура
3) использование холода для разделения газовой смеси
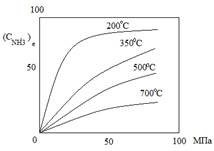
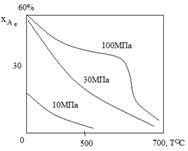
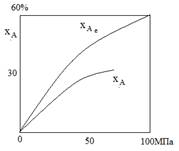
Так как присутствие инертных примесей в реакционной смеси равносильно снижению общего давления, то с увеличением содержания метана, аргона и гелия в смеси скорость реакции синтеза уменьшается.
С повышением содержания аммиака общая скорость реакции падает.
Влияние объемной скорости потока υ.
Увеличение объемной скорости смеси приводит к уменьшению прироста содержания аммиака и, тем самым к росту средней скорости и повышению производительности процесса.
υV=υ/V=1/τ [час-1]
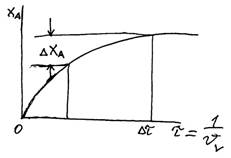
Увеличение υV в 4 раза снижает хА на 20%.
qR= υV*CR=ψAR* υV*CA0*xA
Нарушение автотермичности
Рабочие υV=30*103 1/час
хА=18%
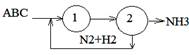
1 – синтез аммиака
2 – выделение аммиака
Реакция синтеза аммиака обратима, поэтому полного превращения азота и водорода в аммиак за время их однократного прохождения через аппарат не происходит. Для более полного использования реагентов необходима их многократная циркуляция через колонну синтеза.
Устройство колонны синтеза.
Особенности:
- надежность
- прочность (320 атм.)
- оптимальный температурный режим
- использование избыточного тепла
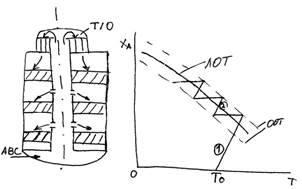
АВС – для снижения температуры
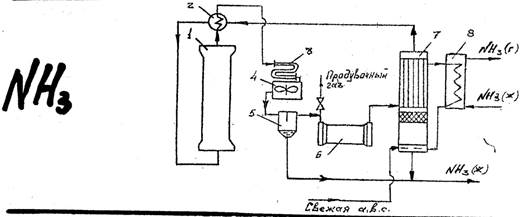
1 – колонна синтеза
Давление 30 МПа
8 – аммиачный холодильник.
Чтобы выделить аммиак, азотоводородную смесь вместе с аммиаком охлаждают до температуры сжижения аммиака. Концентрация аммиака в азотоводородной смеси, содержащей инертные газы, в состоянии насыщения при давлении 30 МПа и различных температурах:
| Т, ᵒС | -10 | |||||
| СNH3, % | 2,1 | 3,2 | 4,7 | 5,5 | 7,3 |
СNH3 – остаточное в газе (то, что остается и не конденсируется).
Поэтому целесообразно в систему подавать жидкий аммиак, который охлаждает газ до -10ᵒС
Часть газа накапливается (Ar) и поэтому от них надо избавляться. Это делается путем сбрасывания продувки. 7% нашего газа сбрасывается в трубу и сжигается.
Свежий газ (азото-водородная смесь) после очистки от посторонних примесей и после охлаждения поступает нижнюю часть конденсационной колонны 7 для очистки от остаточных примесей СО2, Н2О. Свежий газ барботирует через слой сконденсировавшегося жидкого аммиака, особождается от водяных паров и следов СО2, насыщается аммиаком и смешивается с циркуляционным газом. Полученная смесь проходит по трубкам теплообменника конденсационной колонны и нагревается в теплообменнике 2, протекая по трубам. Затем поступает в колонну синтеза 1. В колонне синтеза 1 газ проходит снизу вверх по кольцевой щели между корпусом колонны и поступает в межтрубное пространство внутреннего теплообменника, размещенного в горловине колонны синтеза. В теплообменнике циркуляционный газ нагревается до температуры начала реакции и затем проходит четыре слоя катализатора, концентрация аммиака в газе увеличивается. Пройдя через центральную трубу азотоводородно-аммиачная смесь направляется во внутренний теплообменник, где охлаждается до 300ᵒС. Дальнейшее охлаждение в теплообменнике 3, в трубном пространстве теплообменника 2 холодным циркуляционным газом. Часть аммиака конденсируется. Жидкий аммиак, сконденсировавшийся при охлаждении, отделяется в сепараторе 6, смешивается с жидким аммиаком из конденсационной колонны 8 и из нижней ее части.
Циркуляционный газ поступает в систему вторичной конденсации, поступает в колонну 8 охлаждается до 18ᵒС за счет аммиака охлажденного в аммиачной колонне 8. В сепарационной части колонны 8 происходит отделение жидкого аммиака от газа и смешение свежей АВС с циркуляционным газом.
 2015-08-13
2015-08-13 2034
2034