1) Активный центр (АЦ)
2) Аллостерический центр (АлЦ)
3) Кофакторы
1 – АЦ имеют все ферменты
Активный центр – небольшой участок фермента, который образован радикалами аминокислотных остатков, которые на уровне третичной структуры формируют центр взаимодействия с субстратом (центр, комплементарный субстрату).
Комплементарность – геометрическое (пространственное) и электростатическое (по заряду) соответствие между активным центром и субстратом.
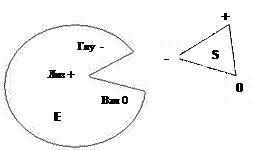 Радикалы аминокислот, которые участвуют в образовании активного центра, могут находиться на расстоянии друг от друга в полипептидной цепи, но при формировании активного центра они сближаются.
Радикалы аминокислот, которые участвуют в образовании активного центра, могут находиться на расстоянии друг от друга в полипептидной цепи, но при формировании активного центра они сближаются.
 |
Активный центр состоит из двух участков:
· Якорный – в который прикрепляется субстрат
· Каталитический – для химического превращения субстрата.
В момент взаимодействия активного центра и субстрата между ними возникают слабые нековалентные связи.
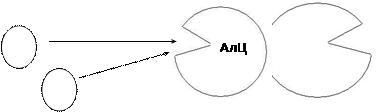
2 - АлЦ – (есть не у всех ферментов) = регуляторный центр, т.к. к нему могут присоединяться активаторы и ингибиторы и регулировать активность ферментов.
АлЦ и АЦ должны быть пространственно разделены: АЦ в одной субъединице, АлЦ - в другой.
Следовательно, аллостерические ферменты – олигомерные белки (четвертичная структура)
а
и
Субъединица с АлЦ – регуляторная. Субъединица с АЦ – каталитическая.
NB!: Аллостерические ферменты катализируют ключевые реакции метаболических путей.
3 – Кофакторы – вещества небелковой природы, необходимые для проявления активности ферментов (есть не у всех ферментов)
· Ионы металлов
· Коферменты
А) Ионы металлов:
· Прочно связываются с ферментом, участвуют в формировании АЦ → металлоферменты (алкогольдегидрогеназы - Zn)
· Непрочно связаны с ферментом, не участвуют в образовании АЦ. Но в присутствии металлов активность ферментов повышается → ферменты, активируемые металлами (α-амилаза слюны – Са2+).
Б) Коферменты
· Производные витаминов
· Участвуют в ферментативных реакциях
· Переносят различные группы
· В ходе ферментативных реакций претерпевают изменения, противоположные изменениям в субстрате.
| ВИТАМИНЫ | Коферментная формула | Что переносит |
| В1 = тиамин | ТПФ (тиаминпирофосфат) | СО2 |
| В2 = рибофлавин | ФАД (флавинадениндинуклеотид) | 2Н (2е- + 2Н+) в ОВР |
| ФМН (флавинмононуклеотид) | ||
| РР = никотинамид | НАД+ (никотинамидадениндинуклеотид), НАДФ | 2Н (2е- + 2Н+) в ОВР |
| В6 = пиридоксин | ПФ (пиридоксальфосфат) | NН2 |
Если в реакции субстрат будет окисляться (т.е. от него отщепляется 2Н), то кофермент будет восстанавливаться.

S- 2H S
 2015-08-13
2015-08-13 445
445








