При написании электронных формул атомов элементов указывают энергетические уровни (значения главного квантового числа n в виде цифр – 1, 2, 3 и т.д.), энергетические подуровни (значения орбитального квантового числа l в виде букв – s, p, d, f) и цифрой вверху указывают число электронов на данном подуровне.
Первым элементом в таблице Д.И. Менделеева является водород, следовательно, заряд ядра атома Н равен 1, в атоме только один электрон на s -подуровне первого уровня. Поэтому электронная формула атома водорода имеет вид:
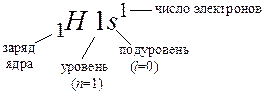
Вторым элементом является гелий, в его атоме два электрона, поэтому электронная формула атома гелия – 2 Не 1 s 2. Первый период включает в себя только два элемента, так как заполняется электронами первый энергетический уровень, который могут занять только 2 электрона.
Третий по порядку элемент – литий – находится уже во втором периоде, следовательно, у него начинает заполняться электронами второй энергетический уровень (об этом мы говорили выше). Заполнение электронами второго уровня начинается с s -подуровня, поэтому электронная формула атома лития – 3 Li 1 s 22 s 1. В атоме бериллия завершается заполнение электронами s -подуровня: 4 Ве 1 s 22 s 2.
У последующих элементов 2-го периода продолжает заполняться электронами второй энергетический уровень, только теперь электронами заполняется р -подуровень: 5 В 1 s 22 s 22 р 1; 6 С 1 s 22 s 22 р 2 … 10 Ne 1 s 22 s 22 р 6.
У атома неона завершается заполнение электронами р -подуровня, этим элементом заканчивается второй период, в нем восемь электронов, так как на s - и р -подуровнях могут находиться только восемь электронов.
У элементов 3-го периода имеет место аналогичная последовательность заполнения электронами энергетических подуровней третьего уровня. Электронные формулы атомов некоторых элементов этого периода имеют вид:
11 Na 1 s 22 s 22 р 63 s 1; 12 Mg 1 s 22 s 22 р 63 s 2; 13 Al 1 s 22 s 22 р 63 s 23 p 1;
14 Si 1 s 22 s 22 р 63 s 23 p 2;…; 18 Ar 1 s 22 s 22 р 63 s 23 p 6.
Третий период, как и второй, заканчивается элементом (аргоном), у которого завершается заполнение электронами р –подуровня, хотя третий уровень включает в себя три подуровня (s, р, d). Согласно приведенному выше порядку заполнения энергетических подуровней в соответствии с правилами Клечковского, энергия подуровня 3 d больше энергии подуровня 4 s, поэтому у следующего за аргоном атома калия и стоящего за ним атома кальция заполняется электронами 3 s –подуровень четвертого уровня:
19 К 1 s 22 s 22 р 63 s 23 p 64 s 1; 20 Са 1 s 22 s 22 р 63 s 23 p 64 s 2.
Начиная с 21-го элемента – скандия, в атомах элементов начинает заполняться электронами подуровень 3 d. Электронные формулы атомов этих элементов имеют вид:
21 Sc 1 s 22 s 22 р 63 s 23 p 64 s 23 d 1; 22 Ti 1 s 22 s 22 р 63 s 23 p 64 s 23 d 2.
В атомах 24-го элемента (хрома) и 29-го элемента (меди) наблюдается явление, называемое «проскоком» или «провалом» электрона: электрон с внешнего 4 s –подуровня «проваливается» на 3 d –подуровень, завершая заполнение его наполовину (у хрома) или полностью (у меди), что способствует бóльшей устойчивости атома:
24 Cr 1 s 22 s 22 р 63 s 23 p 64 s 13 d 5 (вместо …4 s 23 d 4) и
29 Cu 1 s 22 s 22 р 63 s 23 p 64 s 13 d 10 (вместо …4 s 23 d 9).
Начиная с 31-го элемента – галлия, продолжается заполнение электронами 4-го уровня, теперь – р –подуровня:
31 Ga 1 s 22 s 22 р 63 s 23 p 64 s 23 d 104 p 1…; 36 Кr 1 s 22 s 22 р 63 s 23 p 64 s 23 d 104 p 6.
Этим элементом и завершается четвертый период, который включает в себя уже 18 элементов.
Аналогичный порядок заполнения электронами энергетических подуровней имеет место в атомах элементов 5-го периода. У первых двух (рубидия и стронция) заполняется s –подуровень 5-го уровня, у последующих десяти элементов (с иттрия по кадмий) заполняется d –подуровень 4-го уровня; завершают период шесть элементов (с индия по ксенон), в атомах которых происходит заполнение электронами р –подуровня внешнего, пятого уровня. В периоде тоже 18 элементов.
У элементов шестого периода такой порядок заполнения нарушается. В начале периода, как обычно, находятся два элемента, в атомах которых заполняется электронами s –подуровень внешнего, шестого, уровня. У следующего за ними элемента – лантана – начинает заполняться электронами d –подуровень предыдущего уровня, т.е. 5 d. На этом заполнение электронами 5 d -подуровня прекращается и у следующих 14 элементов – с церия по лютеций – начинает заполняться f -подуровень 4-го уровня. Эти элементы включены все в одну клетку таблицы, а внизу приведен развернутый ряд этих элементов, называемых лантаноидами.
Начиная с 72-го элемента – гафния – по 80-й элемент – ртуть, продолжается заполнение электронами 5 d –подуровня, и завершается период, как обычно шестью элементами (с таллия по радон), в атомах которых заполняется электронами р –подуровень внешнего, шестого, уровня. Это самый большой период, включающий в себя 32 элемента.
В атомах элементов седьмого, незавершенного, периода просматривается тот же порядок заполнения подуровней, что описан выше. Предоставляем студентам самим написать электронные формулы атомов элементов 5 – 7-го периодов с учетом всего сказанного выше.
Примечание: в некоторых учебных пособиях допускается другой порядок записи электронных формул атомов элементов: не в порядке их заполнения, а в соответствии с приводимым в таблице количеством электронов на каждом энергетическом уровне. Например, электронная формула атома мышьяка может иметь вид: As 1 s 22 s 22 р 63 s 23 p 63 d 104 s 24 p 3.
 2015-10-16
2015-10-16 6792
6792
