Определение химических показателей, характеризующих
качественное состояние жира рыбы
4.1. Методы выделения липидов из тканей рыбы.
4.1.1. Экстракция липидов хлороформом.
Навеску тщательно измельченной пробы массой 20-50 г обезвоживают путем перемешивания и растирания в фарфоровой ступке с двойным количеством безводного сульфата натрия, затем переносят в гомогенизатор (измельчитель тканей), заливают трехкратным (по объему) количеством хлороформа (свежеперегнанного, химически чистого или медицинского) и ведут экстракцию в течение 5 минут. Хлороформную мисцеллу отделяют от плотного остатка фильтрованием на воронке Бюхнера при разряжении, создаваемом водоструйным или вакуумным насосом. Остаток дважды промывают двукратным количеством хлороформа.
При отсутствии гомогенизатора липиды выделяют настаиванием обезвоженной навески с хлороформом на шуттель-аппарате в течение 40-60 минут с периодическим взбалтыванием вручную.
Для определения в дальнейшем кислотного и перекисного числа непосредственно в хлороформном экстракте (мисцелле) необходимо знать содержание жира в нем. Его определяют следующим образом: весь экстракт переносят в мерную колбу с притертой пробкой, доводят содержимое колбы до метки хлороформом и перемешивают. Из мерной колбы отбирают пипеткой с грушей 5 мл экстракта в предварительно взвешенную с точностью до 0,001 г сухую бюксу. Бюксу помещают на закрытую водяную баню под тягу и выпаривают растворитель. Бюксу с жиром помещают на 20-25 минут в сушильный шкаф с температурой 105-1100С для удаления остатков растворителя, затем охлаждают в эксикаторе и взвешивают.
Содержание жира (Х) в граммах в 1 мл экстракта определяют по формуле:
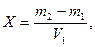
где G1 – масса пустой бюксы, г;
G2 – масса бюксы с жиром, г;
V1 – объем экстракта, взятого для анализа, мл.
Содержание жира в мясе рыбы (L) в % определяют по формуле:
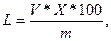
где V – объем всего хлороформенного экстракта, мл;
m – масса навески, взятой для выделения липидов, г;
4.1.2. Экстракция липидов по методу Блайя и Дайера.
Навеску подготовленной пробы взвешивают с точностью до 0,001 г, помещают в сосуд гомогенизатора, туда же добавляют хлороформ, метанол (этанол) и дистиллированную воду в соотношении 1:2:0,8 с учетом воды, находящейся в пробе рыбы. Так, при содержании влаги в пробе 70% к 50 г навески следует добавить 50 мл хлороформа, 100 мл метанола (этанола) и 50*0,8-50*70/100 = 5 мл дистиллированной воды. Полученную навеску обрабатывают в гомогенизаторе при скорости 5000 об/мин в течение 5 мин, затем мисцеллу отфильтровывают на воронке Бюхнера; остаток на фильтре обрабатывают таким же количеством хлороформа, какое было взято для экстракции (в нашем примере 50 мл). Весь фильтрат переносят в делительную воронку с притертой пробкой и добавляют дистиллированную воду (в нашем примере 50 мл) с тем, чтобы окончательное соотношение хлороформа, метанола (этанола) и воды в смеси стало 2:2:1,8. После расслоения смеси на две фазы нижний хлороформный слой с растворенными в нем липидами отделяют и подвергают анализу.
Замерив объем хлороформного экстракта и концентрацию жира в нем, можно определить количественное содержание липидов в рыбе тем же путем, как описано в п. 4.1.1.
4.1.3. Выделение липидов методом центрифугирования.
К измельченной пробе добавляют 18-20 г хлористого натрия на каждые 100 г фарша и тщательно перемешивают. Подготовленный фарш помещают в стаканчики лабораторной центрифуги, которые уравновешивают на технических весах с точностью до 0,1 г и вставляют в гнезда центрифуги. Продолжительность центрифугирования при 5000-6000 об/мин составляет 25-30 мин, при 3000-4000 об/мин – 45 мин.
Отделившийся жир осторожно сливают из стаканчиков в сухую бюксу. Жир должен быть прозрачным, в противном случае его следует профильтровать через складчатый бумажный фильтр и только после этого использовать для анализа.
Содержание жира в мясе рыбы (L) в % определяют по формуле:
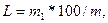
где m1 – масса жира, г;
m – масса фарша, г;
4.2. Определение кислотного числа.
Кислотное число характеризует гидролитическую порчу жира, при которой образуются свободные жирные кислоты. Под кислотным числом понимают количество миллиграммов едкого калия, необходимого для нейтрализации свободных жирных кислот, содержащихся в 1 г исследуемого жира.
Проведение испытания:
Навеску жира, взятую по разности масс с точностью до 0,001 г в количестве 2-10 г (в зависимости от ожидаемого кислотного числа), помещают в коническую колбу емкостью 250 мл, в которую приливают 30-50 мл нейтральной спирто-эфирной смеси, состоящей из одной части этилового спирта и двух частей серного эфира.
При работе с хлороформным экстрактом (мисцеллой) в коническую колбу емкостью 250 мл помещают такое количество мисцеллы, чтобы в ней содержалось 1-2 г жира. К взятому количеству мисцеллы приливают 1-4 части (к массе мисцеллы) спирто-эфирной смеси. Количество добавляемой спирто-эфирной смеси зависит от окраски жира: чем темнее жир, тем больше количество смеси.
К полученному раствору жира прибавляют 1 мл 1%-го спиртового раствора фенолфталеина и титруют 0,1 н раствором гидроксида натрия до появления розовой окраски, не исчезающей в течение минуты.
Кислотное число жира (Кч) в мг КОН/г определяют по формуле:
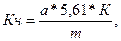
где а – количество 0,1 н раствора щелочи, пошедшей на титрование, мл;
5,61 – количество щелочи, соответствующее 1 мл 0,1 н раствора щелочи, мг;
К – поправочный коэффициент для 0,1 н раствора щелочи;
m – навеска жира или масса жира, содержащегося в объеме хлороформного экстракта, взятого для анализа, г.
Масса жира, содержащегося в 1 мл хлороформного экстракта, определена в п.4.1.1.
Вычисление проводят с точностью до 0,01 мг КОН/г.
4.3. Определение содержания перекисей (перекисного числа).
Количественное определение перекисей основано на реакции их с йодистым калием в уксусно-кислой среде, в результате чего выделяется свободный йод, который оттитровывают серноватистокислым натрием.
Выделение йода перекисями протекает по схеме:
 ROOH + 2 KJ + H2O 2КОН + J2 + ROH
ROOH + 2 KJ + H2O 2КОН + J2 + ROH
Результат определения условно выражают в виде перекисного числа Пч.
Перекисным числом называется количество граммов йода, которое вытесняется из йодистого калия в уксусно-кислой среде под действием перекисей, содержащихся в 100 г жира.
Проведение испытания:
В коническую колбу с притертой пробкой емкостью 250 мл помещают:
- при работе с мисцеллой – 12 мл мисцеллы;
- при работе с жиром – навеску жира около 1 г, взятую по разности с точностью до 0,001 г и 12 мл чистого хлороформа, свободного от перекисей.
Затем в колбу приливают 18 мл ледяной уксусной кислоты, добавляют 1 мл свежеприготовленного насыщенного раствора йодистого калия, закрывают колбу пробкой и, равномерно вращая ее, перемешивают содержимое точно 2 минуты. Затем приливают 100 мл свежепрокипяченной и охлажденной до комнатной температуры дистиллированной воды и 1 мл 1%-го раствора крахмала. Выделившийся йод немедленно титруют 0,01 н раствором серноватистокислого натрия до исчезновения синего окрашивания.
Параллельно проводят контрольный опыт без навески жира.
Количество перекисей (П) в процентах йода определяют по формуле:
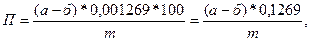
где а – количество 0,01 н раствора серноватистокислого натрия, израсходованного на титрование в рабочем опыте, мл;
б - количество 0,01 н раствора серноватистокислого натрия, израсходованного на титрование в контрольном опыте, мл;
0,001269 – количество йода, соответствующее 1 мл 0,01 н раствора серноватистокислого натрия, г;
m – навеска жира или масса жира, содержащегося в объеме хлороформного экстракта (мисцелле), взятого для анализа, г.
Вычисление проводят с точностью до 0,1% J2.
4.4. Определение содержания карбонильных соединений (альдегидов)
Количественное определение карбонильные соединений основано на измерении интенсивности окраски, развивающейся при взаимодействии альдегидов с бензидином. Результат определений условно выражают в виде альдегидного числа, показывающего содержание карбонильных соединений в расчете на коричный альдегид в миллиграммах на 100 г жира.
Проведение испытания:
При работе с хлороформенным экстрактом жира в сухую чистую пробирку (колбу) с притертой пробкой емкостью 50 мл наливают при помощи пипетки с резиновой грушей 10-15 мл экстракта (в зависимости от ожидаемой степени окисления жира и интенсивности окраски раствора) и равный, точно отмеренный объем этилового спирта.
При работе с жиром, выделенным методом центрифугирования, в мерную колбу емкостью 25 мл отвешивают 0,5-1,2 г жира (с точностью до 0,001 г), растворяют в смеси этилового спирта с хлороформом (1:1) и доводят до метки.
Полученный раствор наливают в кювету шириной 1 см и колориметрируют на фотоэлектроколориметре при длине волны 360 мкм (светофильтр № 2) по отношению к растворителю (спирт + хлороформ). Полученное значение оптической плотности характеризует естественную окраску жира – Д1.
Затем в одну из бюкс с хорошо притертой крышкой отбирают пипеткой 10 мл раствора жира, в другую – 10 мл смеси чистого растворителя (спирт + хлороформ). В каждую бюксу добавляют по 1 мл 0,5%-ного раствора бензидина (в смеси 1:1 этилового спирта и ледяной уксусной кислоты), который готовят на один день. Колбы с содержимым встряхивают и выдерживают 15 мин, после чего определяют оптическую плотность данного раствора жира по отношению к растворителю, обработанному бензидином – Д2. Полученная величина оптической плотности включает плотность самого раствора жира и присутствующих в нем альдегидов.
После каждого определения кюветы следует дважды промыть чистым растворителем (смесь спирта и хлороформа), тщательно протереть ватным тампоном и только после этого заполнить раствором для следующего измерения оптической плотности.
Содержание альдегидов (A) в миллиграммах коричного альдегида на 100 г жира рассчитывают по формуле:
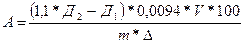 ,
,
где Д1 – оптическая плотность раствора жира до обработки бензидином;
Д2 – оптическая плотность раствора жира после обработки бензидином;
1,1 – поправка на изменение объема после прибавления к 10 мл раствора 1 мл бензидина;
0,0094 – (фактор Ф) – постоянная величина, показывающая, какое количество коричного альдегида приходится на единицу оптической плотности при 360 мкм;
V – объем, в котором растворена навеска жира, мл;
m – навеска жира, г;
Δ – ширина кюветы, см.
Вычисление проводят с точностью до 0,01 мг на 100 г.
 2015-10-16
2015-10-16 1302
1302








