Задание. Дайте термодинамическую характеристику процесса (табл. 21).
Таблица 21
Исходные данные
| Вариант | Уравнение реакции |
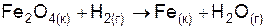 | |
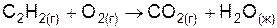 | |
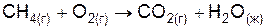 | |
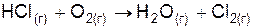 | |
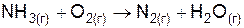 | |
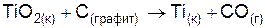 | |
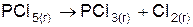 | |
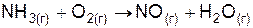 | |
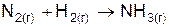 |
Окончание табл. 21
| Вариант | Уравнение реакции |
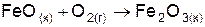 | |
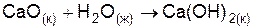 | |
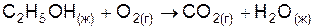 | |
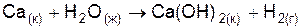 | |
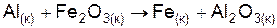 | |
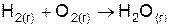 | |
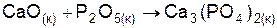 | |
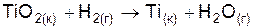 | |
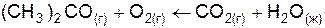 | |
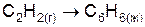 | |
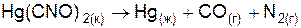 | |
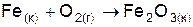 | |
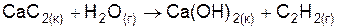 | |
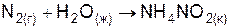 | |
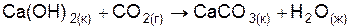 | |
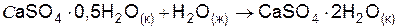 | |
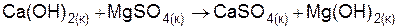 | |
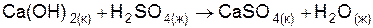 | |
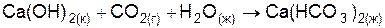 | |
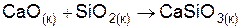 | |
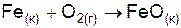 | |
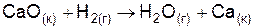 | |
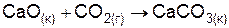 |
Тестовые задания
1. Формулировкой I закона термодинамики является:
а) в реакциях, протекающих при постоянном давлении, изменение энтальпии равно изобарному тепловому эффекту реакции, взятому с противоположным знаком;
б) тепловой эффект реакции зависит от химической природы и агрегатного состояния исходных веществ и продуктов, но не зависит от пути ее протекания;
в) в изолированной системе самопроизвольно протекают процессы в направлении большего беспорядка или наиболее вероятного существования системы;
г) энергия не может ни появляться, ни исчезать, она может только переходить из одного состояния в другое.
2. Реакция невозможна при любых температурах в случае:
а) ΔH > 0, ΔS > 0
б) ΔH > 0, ΔS < 0
в) ΔH < 0, ΔS < 0
г) ΔH < 0, ΔS = 0
3. Указать знак ΔG процесса таяния льда при 273 К:
а) ΔG > 0
б) ΔG = 0
в) ΔG < 0
г) ΔG = ¥
4. Реакция возможна при любых температурах в случае:
а) ΔH > 0, ΔS > 0
б) ΔH < 0, ΔS > 0
в) ΔH < 0, ΔS < 0
г) ΔH = 0, ΔS < 0
5. Укажите, для какого процесса энтропия увеличивается:
а) 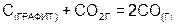
б) 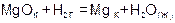
в) 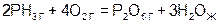
г) 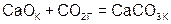
6. Укажите термохимическое уравнение реакции, выражающее эндотермический процесс:
а) 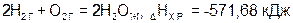
б) 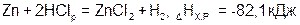
в) 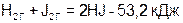
г) 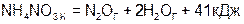
7. С увеличением энтропии протекают процессы:
а) нагревание
б) испарение
в) кристаллизация
г) плавление
д) конденсация
8. В результате реакции, термохимическое уравнение которой 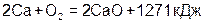 , выделилось 1906,5 кДж, масса кальция, вступившего в реакцию, составила______г.
, выделилось 1906,5 кДж, масса кальция, вступившего в реакцию, составила______г.
а) 40
б) 80
в) 120
г) 135
9. Максимальное значение энтропии имеет:
а) С(алмаз)
б) С(графит)
в) СО2(Г)
г) СО(Г)
10. Тепловой эффект реакции зависит от начального и конечного состояния системы и не зависит от ее промежуточных состояний, закон _________.
 2015-10-22
2015-10-22 995
995








