Слабые электролиты диссоциируют на ионы не полностью, обратимо: 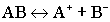 .
.
Диссоциация слабых электролитов имеет две количественные характеристики:
1) λ - степень диссоциации. Степень диссоциации не является константой, она зависит от:
· от температуры (прямая зависимость);
· от концентрации раствора (обратная зависимость).
2) Константа диссоциации - это, по сути, константа равновесия обратимой реакции. Кр=КД=[A+]р*[B+]р/[AB]р.
Константа диссоциации изменяется с температурой, причём зависимость прямая. От концентрации растворов константа диссоциации не зависит.
Многие слабые электролиты диссоциируют ступенчато. Каждая ступень имеет свою константу диссоциации
 .
.
По первой ступени диссоциация заметна при нормальных условиях. Диссоциация по второй ступени заметна при повышенной температуре, при температуре кипения. Всегда Кд1>Кд2>Кд3
Сr(OH)3
 .
.
 2018-01-21
2018-01-21 589
589








