На поверхности жидкостей могут адсорбироваться частицы веществ растворенных в жидкостях. Адсорбция сопровождает процесс растворения, влияя на расщепление частичек растворенного вещества между поверхностным слоем растворителя и внутренним его объемом.
Дж.Гиббс вывел уравнение, связующе величину адсорбции со способностью растворенного вещества изменять поверхностное натяжение раствора.
Г = 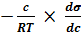 где Г – количество адсорбированного вещества, моль/м2; с – молярная концентрация растворѐнного вещества, моль/дм3, T – температура, при которой происходит адсорбция, R – газовая постоянная,
где Г – количество адсорбированного вещества, моль/м2; с – молярная концентрация растворѐнного вещества, моль/дм3, T – температура, при которой происходит адсорбция, R – газовая постоянная, 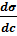 - поверхностная активность.
- поверхностная активность.
Уравнение Гиббса отражает следующую зависимость: чем сильнее уменьшается поверхностное натяжение с увеличением концентрации адсорбируемого вещества, тем больше его поверхностная активность. Это свидетельствует о том, что знак «минус» указывает на обратную зависимость между величиной адсорбции Г и поверхностным натяжением σ. Если 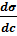 < 0 то Г > 0, т.е. адсорбция положительна (вещество накапливается на поверхности раздела фаз), это характерно для ПАВ. Если же
< 0 то Г > 0, т.е. адсорбция положительна (вещество накапливается на поверхности раздела фаз), это характерно для ПАВ. Если же 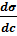 > 0, то Г < 0, т.е. адсорбция отрицательна (вещество накапливается в объѐме), это характерно для ПИВ.
> 0, то Г < 0, т.е. адсорбция отрицательна (вещество накапливается в объѐме), это характерно для ПИВ.
 2018-01-21
2018-01-21 1133
1133
